Исходная концентрация - реагент
Cтраница 3
Скорости прямой и обратной реакции неодинаково зависят от перечисленных выше условий, поэтому соответствующим подбором температуры, давления и исходной концентрации реагентов можно увеличить равновесный выход. Например, если реакция протекает с поглощением тепла, то равновесный выход продукта при повышении температуры увеличивается. Среди обратимых реакций имеются такие, для которых достижение условий равновесия неблагоприятно сказывается на увеличении выхода продукта. [31]
 |
Изменение энергии реагирующей системы при некаталитической ( / и каталитической ( 2 реак. [32] |
Ускоряющее ров специфично отличается от действия других параметров, влияющих на скорость процессов, - температуры, давления, исходной концентрации реагентов, степени перемешивания и др. Повышение температуры, например, это универсальное средство интенсификации, увеличивающее как константу скорости химической реакции, так и коэффициент массопередачи. Но повышение температуры ограничено термостойкостью материалов и смещением равновесия, ведущим к снижению движущей силы экзотермических обратимых процессов. Применение катализаторов - i ускорения химических реакций, не имеющий ограничений и более эффективный; в присутствии катализаторов возможно ускорение химических реакций в миллионы раз. Вследствие изменения механизма реакции в присутствии катализаторов понижается энергия активации. [33]
Это следует из того, что кажущаяся константа скорости второго порядка k остается постоян - - ной, несмотря на изменение исходных концентраций реагентов в 10 - 12 раз. [34]
Нейтрализованные растворы реагента также приводят к существенному снижению натяжения смачивания ( в 2 7 - 8 3 раза в зависимости от исходной концентрации реагента) по сравнению с его значением в случае использования воды ( рис. 3.6, табл. 3.3) использование смесей монокарбоновых кислот в нефтяных коллекторах может обеспечить более полное вытеснение нефти по сравнению с водой. [35]
Исследуем зависимость величины [ MYn ] от величины [ М ] ПОлн, другими словами, рассмотрим, как будет изменяться равновесная концентрация [ MY ] продукта при условии, что сумма исходных концентраций реагентов с остается постоянной. [36]
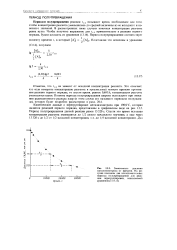 |
Зависимость давления метилизонитрила от времени. На рисунке показаны два последовательных периода полупревращения для реакции перегруппировки, описываемой уравнением. [37] |
Кинетические данные о перегруппировке метилизонитрила при 198 9 С, которая является реакцией первого порядка, представлены в графическом виде на рис. 13.3. Период полупревращения данной реакции равен 13 320 с. Спустя это время исходная концентрация реагента уменьшится до 1 / 2 своего начального значения, а еще через 13 320 с до 1 / 2 от 1 / 2 исходной концентрации, т.е. до 1 / 4 исходной концентрации. [38]
Из этого же условия и значений исходных концентраций реагентов и реакционной смеси рассчитываются концентрации этих реагентов в добавляемых в систему растворах. [39]
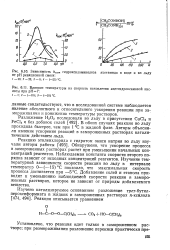 |
Зависимость. каж гидроксиламинолиза ацетамида в воде и во льду от рН реакционной смеси.| Влияние температуры на скорость накопления ацетгидроксамовой кислоты при рН7. [40] |
Обнаружено, что ускорение процесса в замороженных растворах растет при уменьшении начальных концентраций реагентов. Наблюдаемая константа скорости второго порядка зависит от исходных концентраций реагентов. Изучение температурной зависимости скорости реакции во льду в интервале температур 0 - ( - 15) С показало, что максимальная скорость процесса достигается при - 5 С. Добавление солей и этанола приводит к уменьшению наблюдаемой скорости реакции в замороженных растворах, которое не зависит от природы добавляемого вещества. [41]
Время, требующееся для того, чтобы израсходовалась заданная часть, скажем половина, одного из исходных веществ, при различных порядках реакции зависит от первоначальной концентрации реагентов различным образом. Если проведено несколько экспериментов с сильно различающимися исходными концентрациями реагентов, то, сравнивая значения времени полупревращения ( или времени превращения какой-либо иной части, более соответствующей имеющимся экспериментальным данным) в различных экспериментах, можно определить истинный порядок реакции. [42]
Время, требующееся для того, чтобы израсходовалась заданная часть, скажем полоэина, одного из исходных веществ, при различных порядках реакции зависит от первоначальной концентрации реагентов различным образом. Если проведено несколько экспериментов с сильно различающимися исходными концентрациями реагентов, то, сравнивая значения времени полупревращения ( или времени превращения какой-либо иной части, более соответствующей имеющимся экспериментальным данным) в различных экспериментах, можно определить истинный порядок реакции. [43]
В большинстве случаев стараются, однако, так подобрать условия, чтобы равновесную концентрацию реагента можно было приравнять исходной. Это достигается, когда исходная концентрация металла намного меньше исходной концентрации реагента; в этом случае концентрация комплекса, естественно, тоже мала и количеством связанного реагента можно пренебречь. Проводить определение при очень малых концентрациях металла помогает использование радиоактивных изотопов. [44]
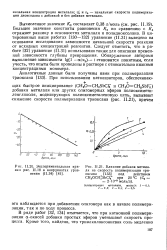 |
Влияние добавок метилаля на скорость полимеризации триоксана под действием CH3OCHjSbCle при 20 С ( С0 2 - 10 - 3 моль / л. [45] |
Страницы: 1 2 3 4