Большая концентрация - электролит
Cтраница 1
Большие концентрации электролитов снижают чувствительность определения конечной точки титрования с крахмалом. Вместо крахмала в тех же условиях рекомендуется применять малахитовый зеленый. [1]
Вследствие большой концентрации электролитов и нагревания хлорид серебра коагулирует и выпадает в виде крупных хлопьев, которые из-за большого содержания азотной кислоты остаются белыми даже на свету; включения в виде темных точек свидетельствуют о присутствии нерастворенного селена. Полученный раствор следует быстро подвергнуть дальнейшей обработки до того, как начнут выпадать кристаллы селенистой кислоты и солей серебра. [2]
При больших концентрациях электролитов q & значительно уменьшается; двойной слой становится похожим на слой Гельмгольца. [3]
При больших концентрациях электролитов значение диэлектрической проницаемости растворов повышается до ее значения для чистого растворителя и становится даже гораздо выше этого значения. [4]
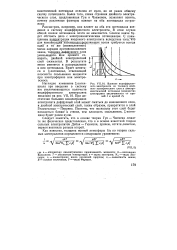 |
Влияние индифферентного электролита на толщину двойного электрического слоя и электрокинетический потенциал ( количество электролита увеличивается от кривой / к кривой 4. [5] |
При до-статочно больших концентрациях электролита диффузный слой может сжаться до моноионного слоя, и двойной электрический слой, таким образом, превратится в слой Гельмгольца - Перрена. Понятно, что поскольку этот слой будет находиться ближе к стенке, чем плоскость скольжения, - потенциал будет равен нулю. [6]
При прибавлении больших концентраций электролита к коллоидном) раствору его ионы отнимают молекулы растворителя от коллоидных частиц. Частицы приобретают свойства лиофобногс коллоида, разрушаются при разряжении, и происходит коагуляция коллоида, называемая процессом высаливания. [7]
При прибавлении больших концентраций электролита к коллоидному раствору его ионы отнимают молекулы растворителя от коллоидных частиц. Частицы приобретают свойства лиофобного коллоида, разрушаются при разряжении, и происходит коагуляция коллоида, называемая процессом высаливания. [8]
Наконец, при больших концентрациях электролита заряд ионного облака приближается к нулю, так как свободные отрицательные заряды поверхностей частиц глины полностью насыщаются катдонами из раствора; соответственно уменьшается гидратация частиц. При этом частицы глины слипаются друг с другом в любых положениях и образуют крупные агрегаты, оседающие в растворе. Эта область высоких концентраций электролита называется областью коагуляции. [9]
При титровании следует избегать больших концентраций электролита, поскольку он может конкурировать с красителем. [10]
Вследствие этого может возникнуть такая большая концентрация электролитов, что произойдет коагуляция. В доказательство правильности этой точки зрения А. В. Ду-манский приводил наблюдения Зигмонди, нашедшего, что коллоидная система при замораживании тем более стойка, чем она устой - - чивее к влиянию электролитов или удалению воды при высушивании. [11]
Натриевые соли этих жирных кислот изостроения требуют гораздо большей концентрации электролита для полного высаливания из водного раствора, чем соответствующие соли нормальных кислот. Мыла разветвленных кислот С12, С13 и С14 не высаливаются даже насыщенным раствором хлористого натрия [18] и теряются в процессе мыловарения с подмыльными щелоками. Таким образом, способность высаливаться зависит не только от молекулярного веса, но и от наличия и длины боковых групп в радикале кислоты. [12]
Для качественного объяснения этого повышения диэлектрической проницаемости при больших концентрациях электролитов принимают, что при таких концентрациях через соединение положительных и отрицательных ионов происходит образование заметного числа новых диполей, которые своей ориентацией производят увеличение диэлектрической проницаемости раствора. [13]
Возможен и третий путь коагуляции: применение сразу же больших концентраций электролита. Это-высаливание гидрофильного коллоида, при котором происходит одновременно и потеря заряда мицелл и их дегидратация. [14]
Он исключительно хорошо растворяется в воде, даже при больших концентрациях электролитов. [15]
Страницы: 1 2 3 4