Молярная концентрация - эквивалент
Cтраница 2
Метод основан на полярографировании свинца в молярной концентрации эквивалента соляной кислоты 3 моль / дм3 при потенциале полуволны от минус 0 43 до минус 0 45 В по отношению к анодной ртути. Присутствие в растворе более 1 мг хрома, молибдена и никеля делает полярографическую волну менее четкой и удобной для измерений. Для устранения влияния хрома последний окисляется до шестивалентного хлорной кислотой, а свинец осаждается на гидроокиси железа аммиаком. Молибден, никель и шестивалентный хром остаются в фильтрате. [16]
Раствор в титриметрическом анализе нередко характеризуют молярной концентрацией эквивалента с поправочным коэффициентом. Поправочный коэффициент равен отношению истинной молярной концентрации эквивалента с ст рабочего раствора к округленной табличной молярной концентрации эквивалента стабл, для которой можно заранее рассчитать, какой массе определяемого вещества соответствует 1 мл рабочего раствора. [17]
Раствор в титриметрическом анализе нередко характеризуют молярной концентрацией эквивалента с поправочным коэффициентом. Поправочный коэффициент равен отношению истинной молярной концентрации эквивалента с ст рабочего раствора к округленной табличной молярной концентрации эквивалента стабл, Для которой можно заранее рассчитать, какой массе определяемого вещества соответствует 1 мл рабочего раствора. [18]
Пользуясь растворами, концентрация которых выражена молярной концентрацией эквивалентов, легко заранее рассчитать, в каких объемных отношениях они должны быть смешаны, чтобы растворенные вещества прореагировали без остатка. [19]
В химическом анализе используют растворы с точно известной молярной концентрацией эквивалента. [20]
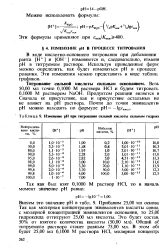 |
Изменение рН при титровании сильной кислоты сильным г и дроке. [21] |
Прибавим 25 00 мл основа Так как молярная концентрация эквивалентов кислоты совпа, с молярной концентрацией эквивалентов основания, то 25 00 гидроксида оттитруют 25 00 мл кислоты. [22]
X в пробе, г; с, - молярная концентрация эквивалента титранта; Кт - объем титранта в точке эквивалентности, мл; Л / ( Х) - молярная масса определяемого вещества X; Лкв ( Х) - фактор эквивалентности вещества X в данной реакции; Ук - вместимость колбы с анализируемым раствором, мл; У - аликвота, взятая на титрование, мл. [23]
Способ громоздкий и менее удобный по сравнению со способом молярных концентраций эквивалента. [24]
Может ли быть молярная концентрация какого-либо раствора больше его молярной концентрации эквивалента и почему. [25]
Таким образом, объемы растворов реагирующих веществ обратно пропорциональны их молярным концентрациям эквивалентов. [26]
Образуется ли осадок SrSO4, если смешать растворы SrQ2 и K2SO4 молярной концентрации эквивалента 0 001 моль / л в равных объемах. [27]
Какой массы дихромат калия потребуется для получения раствора объемом 2 0 л молярной концентрации эквивалента 0 01 моль / л, если он должен использоваться как окислитель в кислой среде. [28]
Чему равен изотонический коэффициент раствора Ca ( NO3) 2, если для него молярная концентрация эквивалента 0 05 моль / л, а осмотическое давление при О С составляет 1 474х105 Па. [29]
Кта - объем титранта, добавленный к моменту эквивалентности; с0 и ст - молярные концентрации эквивалентов ( или нормальные концентрации) титруемого вещества и титранта. [30]
Страницы: 1 2 3 4