Концепция - электроотрицательность
Cтраница 1
Концепция электроотрицательности принята большинством химиков, но точное определение ее едва ли возможно. Первоначальное определение электроотрицательность есть способность атома в молекуле притягивать электроны было дано Полингом. Однако это, как будет видно, не то же самое, что сродство к электрону. [1]
Концепция электроотрицательности до сих пор не приобрела в органической химии такого значения, как понятие о линейных корреляциях свободной энергии ( см. разд. [2]
 |
Радиусы электронных орбит. [3] |
Концепция электроотрицательностей решает задачу количественной характеристики химической связи, как уже говорилось выше, с противоположного конца - со стороны ковалентных веществ. Измерить межатомное расстояние, энергию диссоциации, колебательные частоты и другие характеристики ковалентных молекул типа АА принципиально можно с любой степенью точности. Последнее и позволяет создать количественные характеристики электроотрицательностей атомов и использовать их в различных областях физики, химии и минералогии. В этом и заключается объективное преимущество концепции электроотрицательностей перед теорией поляризации. [4]
Несмотря на то что концепция электроотрицательности плодотворна в качественном отношении, все попытки построить исчерпывающую количественную шкалу оказались неудачными, так как ни одну шкалу не удалось согласовать со всем имеющимся объемом экспериментальных данных. [5]
Следует отметить, что концепция электроотрицательности не является чисто электростатической. Подспудно признается, что заряды переносятся между некоторыми энергетическими уровнями, положение которых зависит от эффективного заряда атома. [6]
Особенно перспективной представляется применение концепции электроотрицательностей в химии силикатов. [7]
Таким образом, анализ концепции электроотрицательностей По-линга приводит к довольно неожиданному и противоречивому выводу. С одной стороны, мы убедились, что фактически имеем здесь дело с приложением ППЛ к энергиям связей. [8]
Мы уже отмечали, что концепция электроотрицательностей основана на принципе аддитивности и в этом ее слабость. [9]
Второй несостоятельной концепцией является так называемая концепция электроотрицательности атомов. Несостоятельность этой концепции также была ясно показана в ряде работ, и эту концепцию мы здесь также рассматривать не будем. [10]
Однако в этой работе критика концепции электроотрицательностей ведется не совсем беспристрастно. [11]
В настоящем параграфе рассмотрены только некоторые приложения концепции электроотрицательностей к химическим проблемам неорганических веществ. Тем не менее автор надеется, что и этот краткий обзор позволит читателю овладеть основными идеями и приемами, которые в свою очередь помогут ему рационально применять учение об электроотрицательностях в общей химии. [12]
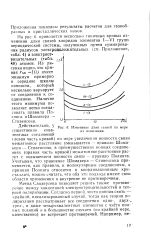 |
Изменение Длин связей по мере их ионизации. [13] |
Метод Сандерсена позволяет решить также противоречие между концепцией электроотрицательностей и теорией поляризации. Согласно первой, чисто ионная связь - крайний, идеализированный случай, тогда как теория поляризации рассматривает все соединения одно -, двух - трех -, и даже четырехвалентных элементов с чисто ион - ных позиций и в большинстве случаев ( по крайней мере, качественно) не встречает противоречий. [14]
Мы убеждены, что отсутствие математических сложностей в концепции электроотрицательностей облегчит ее проникновение в область экспериментальной химии и будет способствовать повышению теоретического уровня исследований. [15]
Страницы: 1 2 3 4