Концепция - электроотрицательность
Cтраница 2
Предложено много полуэмпирических методов оценки зарядов, основанных на концепции электроотрицательности. При формировании химической связи электронная плотность между атомами А и В смещается до тех пор, пока значения х Для обоих атомов не станут одинаковыми. В первый момент атом с большим значением х сильнее притягивает электроны ( рис. 4.33, а и б; ср. [16]
Для качественного понимания природы химической связи большое значение имеет концепция электроотрицательности атома х - Это мера способности атома к образованию ионных соединений, точнее говоря, ионный характер связи АВ зависит от разности электроотрицательностей двух атомов. [17]
Рассмотрение связей в гетероатомных молекулах обычно проводится на основе концепции электроотрицательности. [18]
Предлагаемая трактовка реакционной способности неорганических соединений с точки зрения концепции электроотрицательностей отличается от ставших классическими способов подхода к той же проблеме с позиций кинетики и термодинамики. [19]
К таким больным местам современной теории Хюккель относит и концепцию электроотрицательности, рассматривая ее очень узко - в той интерпретации и в том изложении, которые придал ей Полинг. Критикуя исходные посылки, расчетные схемы и таблицы электроотрицателыюстсй Полинга, указывая на противоречия и расхождения с опытными данными, Хюккель, кроме того, выдвигает два принципиальных возражения против полииговской шкалы электроотрицательностей. Первое его возражение: в этой шкале устанавливается постоянная электроотрицательность, не зависящая от партнера, с которым данный элемент вступает в связь, но, как пишет Хюккель далее, стоит только отказаться от постулата неизменной элейтроотрицательности, как можно получить выводы, например о полярности связи, которые органику-экспериментатору кажутся совершенно очевидными. Второе возражение относится к размерности электроотрицательности - корню квадратному из энергии: совершенно непонятно, каков физический смысл величины с такой размерностью [ 42, стр. [20]
Однако наряду с этим, наблюдаются эффекты, резко отличные от предсказаний концепции электроотрицательности. [21]
Сказанное, конечно, не снимает другую проблему: найти причину, почему концепция электроотрицательностей, в основе которой также лежат ППЛ и представление об однородном взаимодействии, столь хорошо работающие в случае обычных корреляций с индукционными постоянными, не выдерживает сопоставления с экспериментом. [22]
В отличие от работ, рассмотренных выше, в которых велась конструктивная критика концепции электроотрицательности, с конца 50 - х годов появились высказывания авторов, отвергавших эту концепцию целиком, предлагавших ее исключить из теоретической химии. [23]
В этой связи можно указать на работу Бокия и Бацанова 231 ], в которой с позиций концепции электроотрицательностей ( и структурной химии) рассмотрен общий ход качественного анализа элементов. [24]
Понятия об электроотрицательных и электроположительных элементах используются в органической химии уже сравнительно давно, однако в современном смысле концепция электроотрицательностей стала применяться недавно, после установления зависимостей электроотрицательностей атомов от полярностей и кратностей их связей. [25]
Таким образом, пока что все результаты изучения распределения спиновой плотности методом ЭПР соответствуют предсказаниям, сделанным на основе простого применения концепции электроотрицательности к радикалам, имеющим одинаковое геометрическое строение. [26]
Соединения в этой таблице выписаны в порядке возрастания силы поля центрального атома однотипных комплексов Э0, как следует из периодического закона и концепции электроотрицательности. О, изменяется в пределах 0 27 - 0 63 см3 на каждый ион аммония, закономерно снижаясь ( в ряду аналогичных комплексов) по мере увеличения электроотрицательное центрального атома и, следовательно, уменьшения полярности связи Э - О. [27]
Говоря о влиянии гибридизации на электроотрицательность, в результате чего, например, углерод в С2Ш, С2Ш и С2Ш будет неодинаков, Коулсон замечает: Концепция электроотрицательности начинает сдавать ( to break down) [ 34, стр. [28]
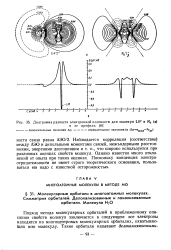 |
Диаграмма разности электронной плотности для молекул LiF и N2 ( a. [29] |
Однако известно много отклонений от опыта при таких оценках. Поскольку концепция электроотрицательности не имеет строго теоретического основания, пользоваться ею надо с известной осторожностью. [30]
Страницы: 1 2 3 4