Координата - реакция
Cтраница 1
 |
Изменение свободной энтальпии бимолекулярной реакции. [1] |
Координата реакции представляет собой геометрическую величину. Она образуется в результате изменения расстояния между реагирующими частицами, связанного с конфигурационными изменениями. При движении вдоль координаты реакции достигается конфигурация переходного состояния. Последняя особенно выгодна для осуществления протекающей при соответствующем элементарном процессе перестройки электронов. Время такой перестройки электронов чрезвычайно мало ( время жизни переходного комплекса), при этом не происходит никаких изменений в молекулярной конфигурации, что связано с большим различием между массой атомов и электронов. На этом основаны приближение Борна - Оппенгеймера и принцип Франка - Кондона. [2]
Координата реакции характеризует путь перехода от реагентов к продуктам химич. В общем случае она не сводится к изменению расстояния между какими-то конкретными атомами в реагирующих молекулах. Высота потенциального барьера, разделяющего реагенты и продукты, называется энергией активации и представляет собой миним. [3]
Координата реакции должна быть типа Bz в первом случае и типа Аг во втором. [4]
Координата реакции имеет только плоскость симметрии. Конфигурация у центрального атома соответственно сохраняется за счет того, что те же самые группы остаются аксиальными. [5]
 |
Структурные параметры и полные энергии для реакции Н - НаСОа. [6] |
Координата реакции - симметрии Cs, и продукт имеет плоскость симметрии. Таким же образом, помимо протона, будут присоединяться к кислороду многие другие кислоты Льюиса. Присоединение слабых нуклеофилов к карбонильной группе усиливается за счет таких взаимодействий. [7]
Координата реакции вблизи области пересечения поверхностей не включает разрыв химической связи. [8]
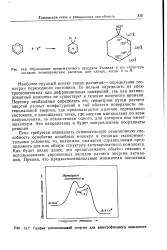 |
Образование промежуточного продукта Уэланда и его структура согласно неэмпирическим расчетам для случая, когда X Н. [9] |
Координата реакции - - 14.7. График потенциальной энергии для электрофильного замещения. [10]
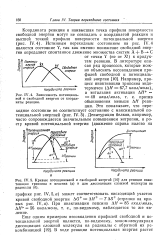 |
Кривые потенциальной и свободной энергий для реакции инактивации трипсина и пепсина ( а и для диссоциации сложной молекулы на радикалы ( б. [11] |
Координата реакции и наивысшая точка профиля поверхности свободной энергии могут не совпадать с координатой реакции и высшей точкой профиля поверхности потенциальной энергии ( рис. IV. [12]
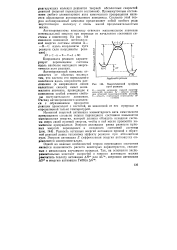 |
Энергетический пути реакции. [13] |
Координата реакции характеризует перемещение системы вдоль наиболее выгодного энергетически пути реакции. [14]
Координата реакции изображена пунктиром, и переходное состояние для некоторого субстрата ( невозмущенное переходное состояние) находится в точке А. [15]
Страницы: 1 2 3 4 5