Координация - лиганд
Cтраница 2
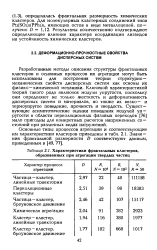 |
Характеристики фрактальных кластеров, образованных при агрегации твердых частиц. [16] |
Результаты количественно подтверждают определяющее влияние характера координации лигандов на устойчивость химических кластеров. [17]
Геометрическая изомерия координационных соединений является следствием различной координации донорных лигандов с центральным атомом металла, что приводит к различной ориентации молекул в электрическом и магнитном полях. Такие комплексы металлов имеют постоянный дипольный момент, величина которого является характеристикой полярности комплекса. Кроме того, существование геометрических изомеров может быть следствием различной ориентации алкильных групп в симметричных бидентатных лигандах, координированных атомом металла. [18]
Изменение геометрической конфигурации и распределения электронной плотности при координации лигандов изменяет и их поведение в химических реакциях. В частности, изменяются кислотно-основные свойства и редокс-потенциал лиганда. [19]
Анализ данных об ЭСКП позволяет делать предсказания об устойчивости и координации лигандов в комплексном ионе. Например, ионы с da и d9 в сильных полях более устойчивы, когда лит ганды координируются с образованием квадратно-плоскостного, а не октаэдрического окружения. Это связано с тем, что ЭСКП в первом случае для них существенно больше, чем во втором. [20]
По-видимому, большая способность Os по сравнению с Ru к координации лигандов обусловливает и большую каталазную активность фтало-цианина осмия. С точки зрения выбранного механизма [22] объясняется действие каталитических ядов NH3 HCN, HF на фталоцианины. [21]
Рассмотрим более подробно изомерию собственно комплексной частицы, если она не вызвана координацией изомерных лигандов. Правда, бывают парадоксальные ситуации, когда констатация изомерии у лиганда зависит от точки зрения на строение комплекса. [22]
В предлагаемом автором определении одной из основных характеристик является наличие координационного центра и координации лигандов. [23]
По мере увеличения размеров кластера доля наружных атомов скелета, которые способны к координации лигандов, либо остается постоянной, либо уменьшается. [24]
Из общего класса циклических соединений выделяют группу внутрикомплексных соединений, которые образуются при координации лигандов комплексонов как по донорно-акцептор-ному механизму, так и с участием неспаренных валентных электронов. В молекуле комплексона имеется несколько функциональных групп, способных одновременно связывать центральный ион ( захватывать его, подобно клешням) с образованием комплесонатов. [25]
Максимальное значение координационного числа показывает, каким пределом ограничена способность центрального атома К координации различных лигандов. [26]
Даже после полного заполнения внут-з а скобкамм ренней сферы в соответствии с максимальным координационным числом комплексные соединения остаются способными к дальнейшей координации лигандов. [27]
К комплексам можно отнести химические соединения, состоящие из ионов или молекул, способных к самостоятельному существованию, и образующихся в результате координации лигандов к центральному атому. Эти соединения в равной степени называют и координационными. [28]
При повышении температуры или под действием водоотнимаю-щих веществ ( СаСЬ, спирт и др.) окраска гидратированных ионов Со2 меняется, что связано с изменением характера координации лигандов и появлением многоядерных комплексов. [29]
При нагревании или под действием водоотнимающих средств ( СаС12, спирт и др.) окраска кристаллогидратов Со ( II) меняется, что связано с изменением характера координации лигандов и появлением многоядерных комплексов. [30]
Страницы: 1 2 3 4