Фронтальная атака
Cтраница 2
Квантово-химические расчеты показывают, что различие энергий переходных состояний при тыловой и фронтальной атаке Nu достаточно велико ( до 20 ккал / моль), чтобы считать абсолютно надежным вывод об инверсии конфигурации при 5 2-за-мещении у насыщенного атома углерода. Реакция 5 2 является согласованным процессом одновременного разрыва связи С-Z и образования связи C-Nu, поэтому аналогично другим согласованным реакциям ( гл. [16]
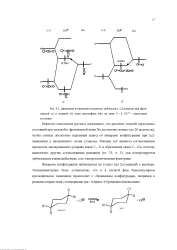 |
Диаграмма возмущения граничных орбиталей в й - реакции при фронтальной ( а и тыловой ( б атаке нуклеофила ( Nu на связь С-Z. ПС - переходное состояние. [17] |
Квантово-химические расчеты показывают, что различие энергий переходных состояний при тыловой и фронтальной атаке Nu достаточно велико ( до 20 ккал / моль), чтобы считать абсолютно надежным вывод об инверсии конфигурации при S l - замещении у насыщенного атома углерода. Реакция SV2 является согласованным процессом одновремеииого разрьша связи С-Z и образования связи С-Nu, поэтому аналогично другим согласованным реакциям ( гл. [18]
Крупные компании со значительными ресурсами и явными конкурентными преимуществами используют стратегии фронтальной атаки. [19]
Реакции характеризуются высокой степенью сохранения конфигурации, что является указанием на фронтальную атаку. [20]
Применение шаростержневых моделей для описания процесса электрофиль-ного замещения в оптически активном металлоорганическом соединении путем фронтальной атаки и атаки с тыла. [21]
Такое определение цис - и транс-атаки может использоваться при обсуждении любых геометрических структур и потому предпочтительнее понятий фронтальная атака и атака с тыла. Однако в случае торакс-атаки г ис-изомер дает смесь цис - и транс - - изомеров, в то время как торакс-изомер дает только ifuc - продукт. Предположение, что торакс-замещение в траке-изомере дает только г мс-изомер, является характерной чертой этого процесса по сравнению с другими процессами, которые будут рассмотрены ниже. [22]
Более того, даже если данные о конфигурации имеются, может оказаться, что предположение о невозможности фронтальной атаки недостаточно убедительно. Во всяком случае, нет никаких оснований a priori утверждать, что фронтальная атака не может произойти в активном центре, локализованном в расщелине белковой молекулы, даже если для свободного раствора такой механизм кажется необычным. [23]
Он уже внутренне созрел, подготов лен к глубокому проникновению в этот новый для физики мир, к фронтальной атаке на его твердыни. [24]
В таких соединениях ( см. рисунок) структура координированного внутримолекулярно ЭОС при действии недиссоциированной полярной молекулой будет способствовать фронтальной атаке реагирующей связи ЭОС в случае органосила-нов ( механизм S. Образование же конечных продуктов будет сильно зависеть от силы взаимодействия М - - - Х в переходном комплексе и в исходной молекуле, а также от многих других условий реакции и взаимодействия центрального атома с внутри - и внешнесферными ли-гандами в переходном комплексе: при Y H, например, в исходном соединении в мягких условиях почти во всех случаях имеет место нуклеофильное замещение. [25]
 |
Высшая занятая молеку - [ IMAGE ] - 26. Возможные направления лярная орбиталь толуола, электрофильной атаки на толуол. [26] |
Интересный случай представляет ароматическое электрофиль-ное замещение, для которого можно показать, что только некоторые определенные центры доступны для фронтальной атаки. [27]
Хлорсульфит-анион распадается затем на SOg и Cl, причем распад происходит настолько быстро, что С1 - может осуществлять фронтальную атаку карбониевого иона до того, как этот ион успеет оказаться сплющенным до плоского состояния. В результате образуется продукт, конфигурация которого не отличается от Конфигурации исходного соединения. Если же проводить реакцию в присутствии основания, например пиридина, то хлористый водород, выделяющийся при образовании хлорсуль-фита на стадии ( 1), дает анион С1 -, который затем легко атакует соединение VIII с задней стороны с удалением - OSOCl. [28]
Хлорсульфит-анион распадается затем на SU2 и С1 -, причем распад происходит настолько быстро, что С1 - может осуществлять фронтальную атаку карбониевого иона до того, как этот ион успеет оказаться сплющенным до плоского состояния. В результате образуется продукт, конфигурация которого не отличается от Конфигурации исходного соединения. Теперь это будет уже реакция SN2 обычного типа, сопровождающаяся обращением конфигурации, а реакция, протекающая по несколько необычному механизму, условно названному механизмом внутреннего нуклеофильного замещения и обозначаемому SNi ( при котором конфигурация исходного вещества сохраняется), больше наблюдаться не будет. [29]
Интересно отметить, что апокамфанол не реагирует [10] также с тионил-хлоридом, хотя эта реакция должна была бы протекать по 5л - г - механизму, включая разложение хлорсульфитного производного в результате фронтальной атаки. Как уже упоминалось, такое взаимодействие, вероятно, связано с образованием ионной пары [18] и ему в случае апокамфанола препятствует высокая энергия образования апокамфил-катиона. Здесь дополнительная движущая сила, обусловленная выделением стабильной молекулы азота, по-видимому, преодолевает помехи, вызванные неустойчивостью иона карбония. Спирты с большими циклами и гидроксилом в голове моста, такие, как бицикло - [3,2,2] - нонанол-1 [ 19а ] и 1-оксиадамантан [ 13а ] ( рис. 13 - 6), все же реагируют с тио-нилхлоридом с образованием соответствующих хлоридов. [30]
Страницы: 1 2 3 4