Коэффициент - влагоемкость
Cтраница 2
Увеличение концентрации гидрофильных сульфо-групп с ростом СПС матрицы находится в полном соответствии с уменьшением в том же направлении коэффициента влагоемкости и эквивалентного коэффициента влагоемкости. [16]
Для характеристики осмотических свойств ионитов, оказывающих большое влияние на их каталитическую активность, важное значение имеют относительная набухаемость и коэффициент влагоемкости. [17]
По величине обменной емкости в расчете на обезвоженное вещество макропористые и гелевые катиониты сходны между собой, но простая связь между коэффициентом влагоемкости и степенью поперечной связанности для них не выполняется. [18]
Главной причиной сжатия пространственной сетки ионита при нагревании его на воздухе автор [229 ] считает отщепление сильно гидратируемых сульфогрупп, причем отмечает, что хотя относительная набухаемость и коэффициент влагоемкости суль-фоионитов понижается симбатно обменной емкости, но для сильно набухающих ионитов изменения указанных величин опережают изменения обменной емкости. Отсюда следует, что нагревание сульфоионитов не только действует на сульфогруппы, но вызывает изменения структуры матрицы ионитов, качественно подобные тем, которые происходят при повышении содержания сшивающего компонента. [19]
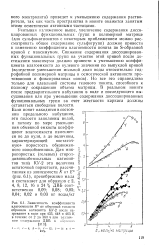
Учитывая изложенное выше, увеличение содержания диссоциированных функциональных групп в полимерной матрице ( для сульфокатионитов с некоторым приближением можно рассматривать общее содержание сульфогрупп) должно привести к изменению коэффициента влагоемкости ионита по S-образной кривой с максимумом. Но все это справедливо только для идеальной системы гелевого ионита, способного к полному сокращению объема матрицы. В реальном ионите после предварительного набухания в воде и последующего высушивания или при уменьшении содержания диссоциированных функциональных групп за счет жесткости каркаса должны оставаться свободные полости. Если ионит находится в состоянии предельного набухания, эти полости заполнены водой, и потому по мере уменьшения обменной емкости коэффициент влагоемкости изменяется не до нуля, а до величины, характеризующей остаточную пористость обезвоженного ионообменника. [21]
Для серийных измерений относительной набухаемо-сти более удобен способ 2, при котором берут две навески гидратированной смолы ( одну - для определения истинной плотности в приборе, вторую - для измерения коэффициента влагоемкости) и навеску смолы, обезвоженной при 110 С, для определения ее плотности в ундекане. При этом способе без разгрузки прибора можно сделать множество параллельных измерений, что вполне компенсирует расход времени на взвешивание. [22]
 |
Относительные потери обменной емкости катионита. [23] |
Коэффициенты КТ и КХ учитывают отношения произведений минимальных величин к максимальным, что вносит неопределенность, так как обменная емкость образцов при нагревании всегда уменьшается, а при облучении и воздействии окислителей может уменьшаться, оставаться неизменной или даже возрастать в зависимости от интенсивности деструкции матрицы и образования новых ( например, карбоксильных) функциональных групп. Коэффициент влагоемкости и удельный объем ионита после опыта также могут изменяться в сторону уменьшения или увеличения. Таким образом, числитель может характеризовать как исходные свойства ионитов, так и свойства их после испытания. [24]
Расчет относительной набухаемости на основании результатов измерений производится следующим образом. При коэффициенте влагоемкости К одному грамму безводной смолы должно соответствовать ( 1 / С) граммов гидратированного-катионита, объем которого равен ( l - - K) V r, где V r - удельный объем гидратированной смолы. [25]
По данным работы [43], коэффициент влагоемкости, определенный этими методами, составил соответственно 1 878; 1 693 и 1 623 г воды на 1 г сухой смолы. Заниженные величины коэффициента влагоемкости в двух последних случаях обусловлены частичной потерей воды из фазы ионита за счет капиллярного высасывания бумагой и удаления с потоком циркулирующего воздуха. [26]
Для оценки изменений в полимерной матрице ионитов при любом воздействии на них пока отсутствуют строгие критерии. Использование для этой цели коэффициента влагоемкости, эквивалентного коэффициента влагоемкости, изменения массы сухого или набухшего вещества после эксперимента может привести к ошибочным выводам о существе и направленности процессов изменения в матрице. Ниже будет показано, что существующий уровень наших знаний в этом вопросе позволяет лишь качественно с помощью комплекса критериев ( изменение обменной емкости коэффициента влагоемкости, массы в сухом и набухшем состоянии, природы выделившихся во внешний раствор продуктов и их количества) установить протекание процессов сшивания, деструкции, разбухания или сжатия за счет структурных превращений и отщепления от матрицы связанных с ней атомов галогенов. В абсолютном большинстве случаев направленность процессов в матрице, к сожалению, остается непредсказуемой. [27]
Методы определения обменной емкости и коэффициента влагоемкости ионообменных мембран аналогичны методам, применяемым для исследования гранульных ионитов. При этом избыточную воду удаляют из набухших мембран не центрифугированием, а отжатием между листами фильтровальной бумаги. Среди методов определения электропроводности ионообменных мембран заслуживают внимания два, проводимых в растворах электролитов и воде. [28]
Любое внешнее воздействие на ионообменный материал, приводящее к сшиванию или деструкции полимерной матрицы и уменьшению обменной емкости, сопровождается изменением содержания сорбированного растворителя в ионообменнике, который находится в состоянии предельного набухания. Количество сорбированного растворителя в ионите характеризуется коэффициентом влагоемкости ( сольватации) - массой воды или органического растворителя, приходящейся на 1 г сухой смолы в состоянии предельного набухания. [29]
После термообработки определяли кислотность водных вытяжек а, коэффициент влагоемкости смолы К, выраженный в г НаО / г смолы, и К - в ммолях Н20 / мг-экв. [30]
Страницы: 1 2 3