Коэффициент - активность
Cтраница 1
Коэффициенты активности, полученные по методу UNIFAC, использовались для определения растворимости и условий образования эвтектики Гмелингом и др. [46]; полученные результаты в основном хорошо соответствуют эксперименту. [1]
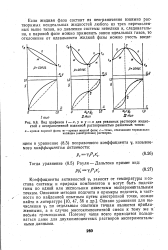 |
Вид графиков t - х, у и у - х для реальных растворов жидкостей с неограниченной взаимной растворимостью различных типов. [2] |
Коэффициенты активностей у зависят от температуры и состава системы и природы компонентов и могут быть подсчй таны по одной или нескольким известным экспериментальным точкам. Однако уравнения для вычисления Yi п отдельным опытньШ точкам являются Приближенными, а в случае многокомпонентной смеси к тому же и весьма громоздкими. Поэтому чаЩе всего приходится польз. [3]
Коэффициенты активности, соответствующие этим фазовым составам, пересчитываются из подходящих уравнений, таких, как NRTL, чтобы проверить оценку, сделанную в начале этого вычисления. Если обнаруживаются значительные расхождения между новым и старым вычислениями, их следует повторять до полной сходимости. [4]
Коэффициенты активности находят экспериментальным путем посредством измерений фазового равновесия или при помощи других методов, описанных в гл. [5]
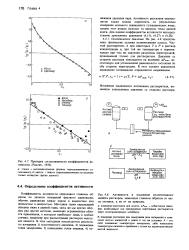
Коэффициент активности у отражает степень взаимодействия ионов, наличие ионных ассоциаций, ионное отталкивание и является функцией минерализации и температуры. [6]
Коэффициент активности у играет важную роль в процессе расчета параметров равновесия жидкость-пар. Однако значения этих величин редко известны. [7]
 |
Проверка согласованности коэффициентов активности ( Редлих, 1976.| Активности и изменение коллигативных свойств растворов, зависящих главным образом от числа молекул, а не от их природы. [8] |
Коэффициенты активности определяют главным образом по данным измерений фазового равновесия, обычно равновесия между паром и жидкостью или жидкостью и жидкостью. Методики таких определений описаны ниже в данной главе, здесь же мы кратко обсудим ряд других методик, имеющих ограниченные области применения, к которым прибегают лишь в особых случаях, например при рассмотрении растворов нелетучих веществ. [9]
Коэффициенты активности можно рассчитать по уравнению (4.59), используя уравнения состояния, применимые как для жидкой, так и для паровой фазы. Однако в настоящее время подобные уравнения состояния охватывают лишь немногие группы веществ; так, уравнение Соава и уравнения, аналогичные уравнению Бенедикта - Уэбба - Рубина, разработаны для класса легких углеводородов и нескольких других газов. [10]
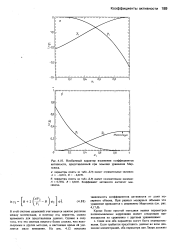 |
Необычный характер изменения коэффициентов активности, представленный при помощи уравнения Мар-гулеса. [11] |
Коэффициент активности достигает максимума. [12]
Коэффициенты активности определены при температурах 300 и 350 К и представлены графически. Полученные кривые свидетельствуют о существенном влиянии температуры в указанном диапазоне. [13]
Коэффициенты активности при бесконечном разбавлении системы ацетон ( 1) хлороформ ( 2) при 1 атм равны 0 37 и 0 46 соответственно. При Xi 0 345 и 64 5 С образуется азеотропная смесь. [14]
Коэффициенты активности рассчитывают непосредственно по уравнениям Маргулеса. Характерные особенности кривых, приведенных на рис. в, - наличие максимумов и минимумов. [15]
Страницы: 1 2 3 4