Коэффициент - активность
Cтраница 2
Коэффициенты активности при заданной температуре определяются уравнениями hi7i 4x1 и 1п72 Вх. Объясните, почему в последнем случае, которому соответствует изоэнтропный состав смеси, давление в системе максимальное. [16]
Коэффициенты активности, полученные по методу UNIFAC, использовались для определения растворимости и условий образования эвтектики Гмелингом и др. [46]; полученные результаты в основном хорошо соответствуют эксперименту. [17]
Коэффициенты активности, соответствующие этим фазовым составам, пересчитываются из подходящих уравнений, таких, как NRTL, чтобы проверить оценку, сделанную в начале этого вычисления. Если обнаруживаются значительные расхождения между новым и старым вычислениями, их следует повторять до полной сходимости. [18]
Коэффициенты активности находят экспериментальным путем посредством измерений фазового равновесия или при помощи других методов, описанных в гл. [19]
Коэффициент активности ( иногда его называют коэффициентом руководства капиталом) говорит о том, насколько активно фирма использует свои капиталы. [20]
Коэффициент активности, у является мерой отклонения реального раствора от закона Рауля и таким образом характеризует степень его неидеальности. [21]
Коэффициент активности зависит от состава, температуры и давления жидкого раствора, а также от выбранного стандартного состояния. Выбор стандартного состояния определяет нормализацию коэффициента активности; если давление, температура и состав, при которых определяется fL, совпадают с параметрами стандартного состояния, то YI должен принять заданное фиксированное значение. [22]
Коэффициенты активности являются функциями состава и температуры. В настоящее время имеется большое число эмпирических и полуэмпирических соотношений для описания этой зависимости. К наиболее распространенным относятся уравнения Маргулеса, Ван Лаара, Вильсона, NRTL. Уравнения отличаются предпосылками, исходя из которых они получены, и областями применимости. Так, например, уравнение NRTL получено исходя-йз Двух-жидкостной упорядоченной структуры раствора, пригодное для описания как гомогенных, так и гетерогенных систем. Поскольку уравнения носят полуэмпирический характер, для определения входящих в него параметров требуются как минимум экспериментальные данные по бинарному равновесию. [23]
Коэффициент активности определяется по эмпирическим и полуэмпирическим уравнениям как функция состава и температуры. Несмотря на то что предложено много таких уравнений, применять следует уравнение Вильсона, так как оно имеет два несомненных преимущества: выражает зависимость коэффициента активности от температуры и позволяет провести обобщение для любой многокомпонентной смеси, используя для этого только данные о бинарных составляющих. [24]
Коэффициенты активности определяются по соотношениям, не учитывающим их зависимость от давления и состава паровой фазы. Таким образом, коэффициенты активности являются функцией состава жидкой фазы и температуры. В некоторых случаях, например в уравнении Вильсона, параметры уравнения явно зависят от температуры. В других уравнениях, таких, как уравнение ван Лаара, константы можно считать независящими от температуры или же, при необходимости, учитывать эту температурную зависимость с помощью некоторых эмпирических соотношений. Здесь предлагаются два варианта подпрограммы АСТСО: первый использует уравнение Вильсона, второй - уравнение ван Лаара. Подпрограммы АСТСО учитывают как симметричную, так и несимметричную нормализацию коэффициентов. [25]
Коэффициенты активности являются функцией состава раствора и температуры. Эта функция от состава раствора может быть представлена интерполяционными полиномиальными уравнениями или зависимостями, вытекающими из теорий растворов неэлектролитов. [26]
Коэффициент активности зависит как от концентрации компонентов в смеси, так и от температуры смеси. Имеются уравнения для определения коэффициентов активности как для бинарной, так и для многокомпонентной смесей. [27]
Коэффициенты активности и летучести определяются по специальным диаграммам. [28]
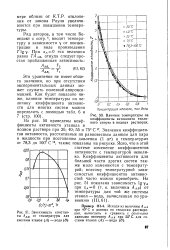 |
Влияние температуры на коэффициенты активности этилового спирта в водных растворах.| Зависимость констан. [29] |
Коэффициенты активности для большей части других систем также мало изменяются с температурой; поэтому температурной зависимостью коэффициентов активностей часто можно пренебречь. [30]
Страницы: 1 2 3 4