Коэффициент - активность
Cтраница 3
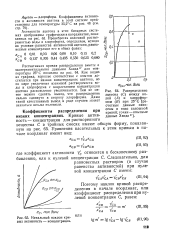
Коэффициенты активности и активности ацетона в этой системе представлены для температуры 35 2 С на рис. 48 ( см. стр. [32]
Коэффициент активности характеризует влияние электростатических сил на способность иона к химическим действиям. Если / 1, то это значит, что движение иона в растворе замедлено. Если же / 1, то ион действует в растворе соответственно своей действительной концентрации. [33]
Коэффициенты активности характеризуют степень отклонения раствора данных жидкостей от идеальной системы. [34]
Коэффициент активности характеризует степень отклонения свойств рассматриваемого компонента в данном растворе от свойств его в соответствующем простейшем растворе. [35]
Коэффициент активности ( фугитивности) газовых смесей определяют по этим диаграммам, исходя из значений псевдокритических параметров, определяемых по формулам гл. [36]
Коэффициент активности в очень разбавленных растворах равен единице ( ас), с увеличением концентрации величина его сначала уменьшается, затем снова начинает возрастать и может стать больше единицы. Таким образом, в очень концентрированных растворах величина активности ионов может быть больше величин концентрации соли. [37]
Коэффициенты активности приняты постоянными и рассматриваются как компоненты кажущихся стандартных констант ско ростей. Отклонение электродного потенциала от равновесного значения обычно относительно мало, и поэтому, если потенциал далек от точки нулевого заряда, ( k0) и а можно считать постоянными. [38]
Коэффициенты активности широко применяются при расчетах любых равновесий в растворах; все термодинамические константы равновесия, используемые практикой, подсчитаны с учетом коэффициентов активности. Коэффициенты активности используются в аналитической химии для оценки влияния посторонней соли на растворимость, особенно труднорастворимых солей. Коэффициенты активности используются также при нахождении нормальных потенциалов Е0 полуэлементов. Обычно значения Е0 отнесены не к единице концентрации, а к единице активности. [39]
Коэффициенты активности у, отнесенные к бесконечно разбавленному раствору этого вещества в спирте же, являются концентрационными коэффициентами активности. Они характеризуют изменение состояния вещества в данном растворителе в связи с изменением его концентрации. Коэффициенты активности у характеризуют изменение состояния вещества как в связи с изменением концентрации, так и в связи с изменением растворителя. Единые нулевые коэффициенты активности у характеризуют изменения энергии вещества при его переходе от бесконечно разбавленного спиртово - vo раствора к бесконечно разбавленному водному раствору. [40]
Коэффициенты активности в неводных растворах могут быть отнесены к бесконечно разбавленному неводному раствору в качестве стандарта [ эти коэффициенты активности мм отмечаем индексом () ] и к единому стандартному состоянию f - Чаще всего в качестве такого стандартного состояния выбирается бесконечно разбавленный водный раствор. Связь между этими коэффициентами активности устанавливается помощью единых нулевых коэффициентов активности Y YoT - Эти коэффициенты активности То показывают различие в энергии вещества в стандартных состояниях. [41]
Коэффициенты активности находятся в зависимости от диэлектрической проницаемости среды. [42]
Коэффициенты активности fo определяются разностью в энергии гидоатмции и сольватации ионов; в данном случае. [43]
Коэффициенты активности ia обозначены инде ксом бесконечности для того, чтобы отметить выбор стандартного состояния. [44]
Коэффициенты активности у характеризуют изменение состояния вещества как в связи с изменением концентрации, так и в связи с изменением растворителя. [45]
Страницы: 1 2 3 4