Коэффициент - активность - отдельный ион
Cтраница 1
Коэффициенты активности отдельных ионов, рассчитанные с помощью соотношений ( V. [1]
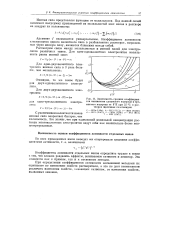 |
Зависимость средних коэффициентов активности хлористого водорода и бромистого водорода от Ym при 25 С в растворах щелочных галогенидов. [2] |
Коэффициенты активности отдельных ионов определить трудно в связи с тем, что сложно разделить эффекты, вызываемые катионом и анионом. Это относится как к прямым, так и к косвенным методам. [3]
Коэффициенты активностей отдельных ионов меняются в зависимости от ионной силы раствора ( /), связанной с величиной заряда ионов и концентрацией электролита. [4]
Коэффициенты активности отдельных ионов нельзя определить опытным путем, но они могут быть вычислены при некоторых допущениях на основании теории сильных электролитов. Согласно этой теории, коэффициент активности / представляет собой меру влияния междуионных сил на способность иона к химическим взаимодействиям. [5]
Коэффициенты активности отдельных ионов не могут быть жспериментально определены. [6]
Коэффициенты активности отдельных ионов зависят от состава раствора, а именно, от вызванной всем имеющимся ионом ионной силы / м - - тг, где т - молярность, a z - валентность отдельных ионов. В табл. 2 приведены значения этих величин, расчитанные из экспериментально найденных значений растворимостей и соответствующих составов растворов. Коэффициенты активности отдельных ионов, соответствующие вычисленным ионным силам растворов, взяты из Льюиса и Рендела [3] или, если это было необходимо, экстраполированы. [7]
Коэффициенты активности отдельных ионов зависят от состава раствора, от ионной силы и, поэтому коэффициент активности находящегося при большом разведении иона Ra, так же как и коэффициент активности иона SO, уменьшается при увеличении общей концентрации раствора. Коэффициенты активности отдельных ионов взяты из сводной таблицы Льюиса и Рендел [4], причем для радия взяты коэффициенты, приведенные для двухвалентного иона. Na SO4 коэффициенты получены экстраполяцией, что можно сделать графическим методом с большой точностью, так как между ] / /, и gy существует почти прямая пропорциональность. Произведение растворимости, напротив, увеличивается почти в 4 раза. [8]
Поскольку коэффициенты активности отдельных ионов термодинамически неопределимы, часто вместо них используют средние коэффициенты активности электролита в целом. [9]
Поскольку коэффициенты активности отдельных ионов термодинамически неопределимы, то часто вместо них используют средние коэффициенты активности электролита в целом. [10]
Определить коэффициенты активности отдельных ионов из опытных данных невозможно. В связи с этим пользуются средней активностью электролита, представляющей собой среднее геометрическое из активностей ионов, составляющих данный электролит. [11]
Хотя коэффициенты активности отдельных ионов, например ТА и ТЕ - т чно не определяются, тем не менее их отношение для одной фазы, скажем Тв / Тд определить можно; соответствующее термодинамическое уравнение можно вывести стро го - см. ниже. [12]
Хотя коэффициенты активности отдельных ионов, например ТА и fB точно не определяются, тем не менее их отношение для одной фазы, скажем 7В / 7А, определить можно; соответствующее термодинамическое уравнение можно вывести строго - см. ниже. [13]
Вычисление коэффициентов активности отдельных ионов можно было бы произвести по коэффициенту активности соли, если известен коэффициент активности второго иона. Тогда, предполагая, что коэффициент активности отдельного иона зависит лишь от ионной силы раствора, можно, переходя от одного электролита к другому ( с общим ионом), вычислить коэффициенты активности отдельных ионов. Такой расчет, в силу некоторой произвольности исходных данных и невозможности распространения правила ионной силы на любые концентрации, не может дать точных результатов, хотя для практических целей весьма удобно считать коэффициенты активности ионов одинаковой валентности приблизительно равнцми, если одинаковы ионные силы растворов. [14]
Вычисление коэффициентов активности отдельных ионов можно было бы произвести по коэффициенту активности соли, если известен коэффициент активности второго иона. Тогда, предполагая, что коэффициент активности отдельного иона зависит лишь от ионной силы раствора, можно, переходя от одного электролита к другому ( с общим ионом), вычислить коэффициенты активности отдельных ионов. [15]
Страницы: 1 2 3 4