Коэффициент - активность - отдельный ион
Cтраница 3
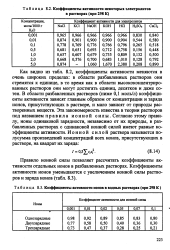 |
Коэффициенты активности некоторых электролитов в растворах ( при 298 К.| Коэффициенты активности ионов в водных растворах ( при 298 К. [31] |
Правило ионной силы позволяет рассчитать коэффициенты активности отдельных ионов в разбавленных растворах. [32]
Правило ионной силы позволяет рассчитать коэффициенты активности отдельных ионов в разбавленных растворах. [33]
В справочниках по химии даются дифференцированные коэффициенты активности отдельных ионов или же для групп ионов. [34]
Это и есть выражение для коэффициента активности отдельного иона. В этом выражении величины е и k постоянные. Для данного электролита величина z остается неизменной; для данного раствора D - также постоянная величина. [35]
Это и есть выражение для коэффициента активности отдельного иона. В этом выражении величины е и k постоянные. Для данного электролита величина z остается неизменной; для данного раствора е - также постоянная величина. [36]
Это и есть выражение для коэффициента активности отдельного иона. В этом выражении величины е и k постоянные. Для данного электролита величина г остается неизменной; для данного раствора е-также постоянная величина. [37]
Электростатическая теория сильных электролитов позволяет вычислить коэффициент активности отдельного иона и средний коэффициент активности сильного электролита. [38]
Используя эти данные, можно рассчитать коэффициенты активности отдельных ионов по уравнениям ( V. [39]
И Меняются для определения активности и коэффициентов активности отдельных ионов. [40]
Аналогично Лейендек-кер [60] вывел выражения для коэффициентов активности отдельных ионов в многокомпонентных системах. [41]
Кроме того, предположительно, равны и коэффициенты активности отдельного иона в двух различных растворах, имеющих одинаковую ионную силу. [42]
 |
Ассоциация NaBrO3 в водно-диоксановых растворах ( вода неограниченно смешивается с диоксаном. [43] |
Уравнение (1.11) представляет собой более общее выражение коэффициента активности отдельного иона, чем выражения, рассмотренные ранее. Ионы, образованные при растворении нитрата калия, не реагируют с ионами цинка, а влияют лишь на их коэффициент активности, который зависит от ионной силы раствора. Электролит, который присутствует в избытке по сравнению с другими растворенными веществами, называется индифферентным, или основным. [44]
Для описания ионообменных равновесий необходимо знать отношение коэффициентов активности отдельных ионов. [45]
Страницы: 1 2 3 4