Температурный коэффициент - растворимость
Cтраница 2
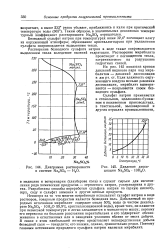 |
Давление диссоциации NaaSO4 10Н2О. [16] |
Таким образом, в значительных диапазонах температурный коэффициент растворимости Na2SO4 отрицателен. [17]
В настоящей статье приводятся расчетные данные температурного коэффициента растворимости Не, Ne и Аг в воде, органических растворителях и водно-органических системах в интервале температур от 10 до 70 С. [18]
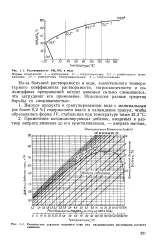 |
Растворимость NH4NO3 в воде.| Равновесное давление водяного пара над насыщенными растворами нитрата аммония. [19] |
Из-за большой растворимости в воде, значительного температурного коэффициента растворимости, гигроскопичности и полиморфных превращений нитрат аммония сильно слеживается, что затрудняет его применение. [20]
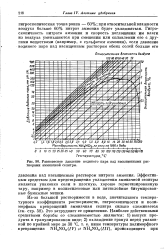 |
Равновесное давление водяного пара над насыщенными растворами аммиачной селитры. [21] |
Из-за большой растворимости в воде, значительного температурного коэффициента растворимости, гигроскопичности и полиморфных превращений аммиачная селитра сильно слеживается ( см. стр. Это затрудняет ее применение. [22]
Как уже отмечалось в главе I, температурный коэффициент растворимости ( ТКР) солей, образующих системы 2-го типа, во всем температурном интервале или начиная с некоторых температур отрицателен, вследствие чего концентрация насыщенных растворов таких солей при температурах, приближающихся к критической температуре воды, становится очень незначительной. Давление пара насыщенных растворов таких солей, в особенности при высоких температурах, близко к давлению пара чистой воды; соответствующие кривые, в отличие от солей 1-го типа, максимума не имеют и заканчиваются в критической точке, параметры которой, вследствие малой растворимости соли, должны быть близки к критическим параметрам чистой воды. [23]
В главе I уже отмечалось, что температурный коэффициент растворимости солей, образующих системы 1-го типа, положителен. Вследствие этого при достаточно высоких температурах такие соли могут образовывать весьма концентрированные растворы, в которых критические явления отсутствуют. [24]
В этих системах отрицательный в чистой воде температурный коэффициент растворимости карбоната натрия, ор-тофосфата натрия и фторида натрия 4 переходит в положительный в растворах электролитов. [25]
В этой работе отмечено также изменение знака температурного коэффициента растворимости с отрицательного на положительный при давлениях выше 800 - 850 атм. [26]
Пользуясь этим приемом высаживания избытка соли при помощи температурного коэффициента растворимости, мы получаем конечный раствор той же концентрации, как и исходный, что имеет большое значение при изучении распределения, так как при изменении состава раствора меняется константа распределения. [27]
Для методов кристаллизации при химической реакции и при испарении температурный коэффициент растворимости не имеет значения. Что касается метода концентрационной конвекции, то чем больше температурный коэффициент растворимости вещества, тем легче интенсифицировать процесс выращивания. Поэтому линия, ограничивающая область применения этого метода в отношении растворимости, должна в принципе отклоняться вверх и влево. Однако недостаток данных не позволил провести ее точнее, чем это сделано на графике. [28]
Характеристика легкорастворимых соединений в воде показана на рис. 12.2. Температурные коэффициенты растворимости некоторых из них при температурах воды более 200 С отрицательны. [29]
Однако область концентраций, в которой происходит это изменение температурного коэффициента растворимости, для веществ, очень слабо растворимых в чистой воде, пока еще не установлена. [30]
Страницы: 1 2 3 4