Температурный коэффициент - растворимость
Cтраница 3
Создание пересыщения политермическим способом обычно применяется для соединений со значительным температурным коэффициентом растворимости. [31]
При исследовании политерм растворимости относительно хорошо растворимых солей со значительными температурными коэффициентами растворимости сравнительно часто используют визуалъно-поли-термический метод. [32]
Здесь по осям в логарифмическом масштабе располагается растворимость с и температурный коэффициент растворимости ( 5 при температурах 5 - 65 С взятых в качестве примера 25 выращенных нами веществ. Направление стрелок показывает направление изменения параметров с ростом температуры. Начало и конец стрелок соответствует параметрам при указанных температурах. [33]
Так как исходный маточный раствор бисульфита является насыщенным, а температурный коэффициент растворимости пиросульфита натрия в пределах производственных температур ( 25 - 40) невелик, то при последовательном или одновременном проведении процессов нейтрализации раствора содой и насыщения реакционной массы сернистым газом происходит кристаллизация пиросульфита. Концентпа-ция поступающего в абсорбер сернистого газа может быть любой. Даже при содержании в газе десятых долей процента SO2 при достаточных размерах абсорбционной колонны поглощение SO2 будет практически полным. [34]
Так как исходный маточный раствор бисульфита является насыщенным, а температурный коэффициент растворимости пиросульфита натрия в пределах производственных температур ( 25 - 40) невелик, то при последовательном или одновременном проведении процессов нейтрализации раствора содой и насыщения реакционной массы сернистым газом происходит кристаллизация пиросульфита. Концентрация поступающего в абсорбер сернистого газа может быть любой. Даже при содержании в газе десятых долей процента SO2 при достаточных размерах абсорбционной колонны поглощение SO2 будет практически полным. [35]
Переход от Ne к Аг сопровождается резким скачком растворимости и температурного коэффициента растворимости. [36]
 |
Схемы дробной перекристаллизации. б - с двойным отбором ( по Типсону 1, 21. [37] |
Эта схема особенно ценна, если компонент А обладает высоким значением температурного коэффициента растворимости. [38]
Необходимо отметить, что попытки разделения обменивающихся соединений, основанные на использовании различия температурных коэффициентов растворимости органических производных ртути, приводили лишь к частичным успехам. Возникающие при этом трудности были обусловлены мало изученными явлениями совместной кристаллизации галогенидов ртути с ее неполными органическими производными. [39]
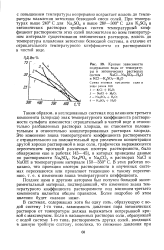 |
Кривые зависимости содержания воды от температуры в эвтонических растворах систем NaCl - Na2SO4 - H2O и КС1 - K2SO4 - Н2О. [40] |
Таким образом, в исследованных системах под влиянием третьего компонента ( хлорида) знак температурного коэффициента растворимости сульфата изменяется: отрицательный в чистой воде и относительно разбавленных растворах хлорида, он становится положительным в относительно концентрированных растворах хлорида. Это изменение знака температурного коэффициента растворимости с отрицательного на положительный при увеличении концентрации другой хорошо растворимой в воде соли, графически выражающееся пересечением проекций различных изотерм растворимости, было обнаружено еще в работах [43-45], в которых приведены данные по растворимости Na2SO4, Na3PO4 и Na2CO3 в растворах NaCl и NaOH в температурном интервале 150 - 350 С. [41]
При выборе растворителя для процесса кристаллизации охлаждением необходимо учитывать как растворяющую способность, так и температурный коэффициент растворимости. Первый фактор определяет объем кристаллизатора, а второй - выход кристаллизующегося растворенного вещества. Часто случается, особенно в водных органических системах, что низкая растворимость сочетается с высоким температурным коэффициентом растворимости. Например, растворимость салициловой кислоты в воде при 20 и 80 С составляет 0 20 и 2 26 г / 100 г соответственно. Следовательно, при охлаждении от 80 до 20 С большая часть растворенного вещества ( 91 %) осаждается и, следовательно, выход кристаллизующегося растворенного вещества высокий. [42]
Позднее нами и другими авторами был получен большой экспериментальный материал, подтвердивший, что изменение знака температурного коэффициента растворимости под влиянием третьего компонента является общим правилом. Более подробно об этом явлении будет сказано ниже. [43]
 |
Технологическая схема выделения хлорида калия из сильвинита флотационным методом. [44] |
Галургический способ выделения хлорида калия из сильвинита или метод избирательного растворения и раздельной кристаллизации основан на различии температурных коэффициентов растворимости хлоридов калия и натрия при их совместном присутствии, то есть в системе КС1 - NaCl-ЩО. [45]
Страницы: 1 2 3 4