Температурный коэффициент - реакция
Cтраница 1
Температурный коэффициент реакции А - В считается положительным, но меньшим, чем коэффициент реакции В - С. Оптимальная температура реакции вначале должна быть высокой, чтобы ускорить первую реакцию и получить больше продукта В в заданном объеме. Однако по мере увеличения количества продукта температуру процесса следует понижать, так как при этом скорость реакции В - С уменьшается в большей степени, чем реакции А - В. Таким образом, протеканию реакции должен соответствовать определенный температурный режим. [1]
Температурный коэффициент реакции понижается с повышением температуры ( табл. 114) ( см. стр. [2]
 |
Температурная зависимость констант скорости реакции образования ( k и разложения ( k йодистого водорода HJ ( по Боден-штейну. [3] |
Температурный коэффициент реакции, определяемый формулой (2.47), представляет некоторое неудобство вследствие его резкой зависимости от температуры. [4]
Температурный коэффициент реакции невелик. При температуре свыше 205 активность катализатора резко снижается. [5]
 |
Скорость окисления расплавленного свинца воздухом при 626. [6] |
Температурный коэффициент реакции сравнительно мал: так, для Т 800 при повышении температуры на 10 скорость окисления увеличивается приблизительно на 13 %, а при повышении температуры от 800 до 900 - приблизительно в 3 2 раза. [7]
Температурный коэффициент реакции в этом случае также мал. [8]
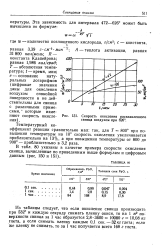 |
Скорость окисления расплавленного свинца воздухом при 626. [9] |
Температурный коэффициент реакции сравнительно мал: так, для Т - 800 при повышении температуры на 10 скорость окисления увеличивается приблизительно на 13 %, а при повышении температуры от 800 до 900 - приблизительно в 3 2 раза. [10]
Температурный коэффициент реакции в допредельной области, вычисленный из найденного уравнения, равен 1 24 в интервале 15 - 25 С и постепенно уменьшается с повышением температуры ( до 1 206 в интервале 35 - 45 С), как это и следует из уравнения Аррениуса. Эта величина выше определенной Майером для золота, так как она относится к допредельной по цианиду области. В области же, контролируемой диффузией кислорода, зависимость скорости от температуры более сложна - с повышением температуры увеличивается скорость диффузии и снижается кинематическая вязкость раствора, но уменьшается и растворимость кислорода. [11]
Температурный коэффициент реакции химической и ферментативной ( Qt0) показывает, во сколько раз ускоряется данная химическая реакция при повышения температуры на 10 С. [12]
Температурный коэффициент реакции очень мал ( 1 09 на 10), что дает для энергии активации наиболее медленной из двух стадий развития цепи значение - 1500 ккал. Такая малая величина энергии активации, естественно, приводит к большому значению длины цепи при комнатной температуре. [13]
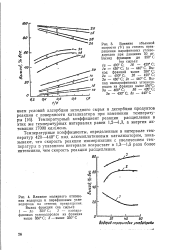 |
Влияние молярного отношения водорода к парафиновым углеводорода на степень превращения. [14] |
Температурный коэффициент реакции расщепления в этих же температурных интервалах равен 1 2 - 1 3, а энергия активации 17000 кал / моль. [15]
Страницы: 1 2 3 4