Температурный коэффициент - реакция
Cтраница 2
Температурные коэффициенты реакции гидрогенизации кислот, вычисленные по изотермам общей степени превращения кислот ( рис. II), оказались равными 1 4 г: ри 200 - - 220 с: С, 1 3 при 220 - 240 С и 1 2 при 240 - 280 С. Эти коэффициенты близки к полученным при гидрогенизации эфиров. [16]
Вычислите температурный коэффициент реакции, если при нагревании системы на 30 градусов скорость реакции увеличивается в 27 раз. [17]
Если температурный коэффициент реакции 1 больше соответствующего коэффициента реакции 2, а коэффициент реакции 3 меньше, чем коэффициент реакции 4, то оптимальная температура должна понижаться вдоль оси реактора. [18]
 |
График зависимости фактора эффективности от модуля при молярной доле реагентов, равной 1 0. [19] |
Поэтому температурный коэффициент реакции в поре может быть меньше, чем на плоской поверхности. [20]
При известном температурном коэффициенте реакции уравнение ( 48а) используется для вычисления энергии активации. При этом следует иметь в виду, что температурный коэффициент не постоянен, а немного уменьшается с ростом температуры. [21]
 |
Зависимость выхода продукта от температуры для экзотермических обратимых про. [22] |
При известном температурном коэффициенте реакции уравнение ( IV77) используется для вычисления энергии активации. При этом следует иметь в виду, что температурный коэффициент не постоянен, а уменьшается с ростом температуры. [23]
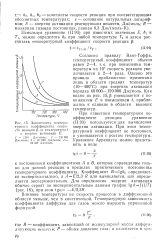 |
Зависимость температурного коэффициента скорости реакции ( 3 от температуры t. [24] |
При известном температурном коэффициенте реакции уравнение (11.93) используется для вычисления энергии активации. При этом температурный коэффициент не постоянен, а уменьшается с ростом температуры. [25]
Чему равен температурный коэффициент реакции, если при увеличении температуры на 50 скорость реакции возросла в 32 раза. [26]
Чему равен температурный коэффициент реакции, если при повышении температуры на 40 ее скорость увеличивается в 256 раз. [27]
Чему равен температурный коэффициент реакции, если при повышении температуры на 50 ее скорость увеличивается в 32 раза. [28]
С учетом температурного коэффициента реакции между K [ PtNHsCl3 ] и NH3, который равен - 2.4, примерное значение коэффициента скорости этой реакции при 15 равно 0.48 - 10 - 3 л / сек-мол. При сравнении его с коэффициентом скорости для соответствующей бромистой системы оказалось, что бромистая соль реагирует в 14 - 15 раз быстрее, чем хлористая. Такое различие в скоростях реакций обусловлено не только различием в реакци-онной способности координат G1 - Pt11 - C1 и Вг-Ptn - Вг, но и тем, что цис-влияние молекулы аммиака на реакционную способность координаты Вг - Pt11 - Вг выражено значительно сильнее, чем в хлористой системе. [29]
Для вычисления температурного коэффициента реакций растворения в тех случаях, когда известна кажущаяся теплоемкость растворенного вещества, достаточно знать лишь теплоемкость этого же вещества в чистом виде. [30]
Страницы: 1 2 3 4