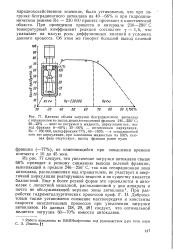
Температурный коэффициент - реакция
Cтраница 3
Покажем, что температурный коэффициент реакции у зависит от температуры. [31]
В ферментативных реакциях температурные коэффициенты реакции обычно ниже, чем в некаталитических реакциях. [32]
Согласно формуле (2.48), температурный коэффициент реакции т ] является постоянным и той мере, в какой энергия активации Е не зависит от температуры. [33]
Третьей важной величиной является температурный коэффициент реакции. Для данной реакции на данном катализаторе константа k увеличивается с температурой, так что величина параметра h также увеличивается с температурой. Однако если при повышении температуры h значительно превышает единицу, то температурный коэффициент начинает падать. [34]
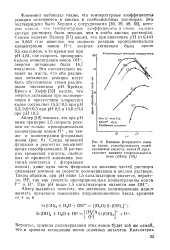 |
Влияние фторидного ион & на время гелеобразования золей кремневой кислоты. линия Н представляет влияние гидроксильнога иона ( Айлер. [35] |
Флемминг наблюдал также, что температурные коэффициенты реакции отличаются в кислых и слабощелочных растворах. Это подтверждено было Хердом с сотрудниками [36, 39, 49, 50], которые нашли, что температурные коэффициенты в очень сильно кислых растворах были меньше, чем в слабо кислых растворах. Совсем недавно Пеннер [51] нашел, что при значениях рН от 0 441 до 0 863 ( где известно, что скорость реакции пропорциональна концентрации ионов Н) энергия активации была около 9 5 ккал / моль, в то время как при рН 4 64, где скорость пропорциональна концентрации ионов ОН -, энергия активации была 16 1 ккал / моль. [36]
 |
Поляризационные кривые [ IMAGE ] Зависимость логарифма тока водородного электрода в серно - от обратной температуры при поля-кислом растворе при различных ризации ( в в. [37] |
По данным работы [21], температурный коэффициент реакции ионизации водорода соответствует 2000 - 3000 кал / моль. [38]
Данные последней графы выражают значения температурного коэффициента реакции, так как опыт во всех трех случаях производится в условиях одинаковой концентрации растворов, а следовательно, отношение величин скоростей реакции должно равняться отношению констант скоростей. [39]
Показано, что реакция бимолекулярна; температурный коэффициент реакции равен 1 6; энергия активации составляет 17500 800 ккал / моль. [40]
Из этих данных следует, что температурный коэффициент реакции сравнительно невелик: на каждые 10 повышения температуры константа k возрастает лишь в 1 135 раза. Это заставляет полагать, что приведенная выше схема не выражает истинного механизма реакции. Ряд признаков свидетельствует о цепном механизме этого процесса. [41]
При энергии активации, равной нулю, температурный коэффициент реакции, скорость которой выражается законом Аррениуса ( что не всегда имеет место), очевидно, равен единице. [42]
Некоторые авторы считали, что предложение о зависимости температурного коэффициента реакции от теплоты реакции, из чего следует, что каждая реакция имеет единственное значение этого коэффициента, носит искусственный характер. [43]
Такие вещества, подобно катализаторам, не изменяющим температурного коэффициента реакции, прочно удерживаются на металлической поверхности. Есть основания предполагать, что они связаны с поверхностью силами специфической адсорбции, а в некоторых случаях-хемосорбции, в результате которой образуется поверхностная пленки продукта реакции. [44]
Страницы: 1 2 3 4