Аминогруппа - аминокислота
Cтраница 3
На удерживание влияет основность используемого капроната, а также комплексообразование между ионом металла и аминогруппой аминокислоты. Замена аминогруппы на N-трифторацетильную группу приводит к заметному уменьшению удерживания на всех фазах. Применение в качестве НЖФ раствора капроната никеля в силиконе дает лучшие результаты по разделению. [31]
В кислой среде из нитрита натрия выделяется свободная азотистая кислота, которая реагирует с аминогруппой аминокислоты. [32]
Взаимодействием бензилового спирта с фосгеном получают карбобензо-ксихлорид - один из самых распространенных агентов для защиты аминогруппы аминокислот в пептидном синтезе. [33]
Вероятно, что начальной стадией реакции Майяра является образование М - замещенных гликозиламинов путем взаимодействия епро-тонироваиной аминогруппы аминокислот, пептидов или белшв с гли-козидным Г идроксилом моносахарида, затем образуется шиффово основание. [34]
Бергман [102] предложил более изящный, но также трудоемкий, ступенчатый синтез полипептидов, при котором защита аминогруппы аминокислот осуществляется при помощи реакции с бензиловым эфиром хлормура-вьиной кислоты. Образующееся N-карбобензилоксипроизводное затем превращают в хлорангидрид или азид кислоты и конденсируют с аминокислотой или пептидом. [35]
Ка ( Ка) - константа кислотности карбоксильных групп аминокислоты; Къ ( Къ) - константа основности аминогрупп аминокислоты; Ку, ( Kw) - ионное произведение воды и произведение активностей ионов воды; / R, / R -, / R - коэффициенты активности ионов и цвиттерионов. [36]
Эта короткая глава посвящена обсуждению химии карбрновых кислот с заместителями, содержащими атомы азота в более высокой степени окисления, чем аминогруппа аминокислот. [37]
Полученные данные свидетельствуют о том, что степень протониза-ции нуклеотидопептидного азота, а следовательно, легкость гидролиза нуклеотидопептидной связи, мало зависит от структуры радикала и основности аминогруппы аминокислоты, участвующей в образовании фосфоамидной связи; значительно большее влияние на скорость и механизм гидролиза оказывают соседние протоно-акцепторные ( делока-лизующие положительный заряд амидного азота) или протонодонорные группировки. [38]
Роль реак-ционноспособной группы в молекуле пиридоксальфосфата играет альдегидная группа. При взаимодействии этой группы с аминогруппой аминокислоты образуется шиффово основание. В процессе трансамини-рования аминогруппа остается связанной с пиридоксальфосфатом, а углеродный скелет аминокислоты отщепляется в виде 2-оксокислоты. Пиродоксальфосфат регенерируется затем в результате реакции с соответствующей оксокислотой. [39]
Трансаминирование является очень важным процессом превращения аминокислот в организме. В этой реакции происходит обратимый перенос - аминогруппы аминокислоты на кетокислоту без промежуточного отщепления аммиака. Реакция протекает наиболее активно, когда один из субстратов представлен дикарбоновой амино-или кетокислотой. Процесс трансаминирования катализируется ферментами - аминотрансферазами, кофермен-том которых является пиридоксальфосфат. Процесс активно протекает в печени, сердечной мышце, скелетных мышцах, почках, семенниках и других органах. В сыворотке крови активность аминотрансфераз очень низка. При нарушении целостности клеточных мембран амино-трансферазы проникают из тканей в кровь. [40]
Декарбоксилирование аминокислот совершается при помощи фермента, состоящего из белка и кофермепта. Он, как альдегид, реагирует с аминогруппой аминокислоты; в результате образуется шиффово основание. [41]
В результате взаимодействия аминокислот с глюкозой и другими моносахаридами образуются СОг и Н О. При взаимодействии аминокислот с моносахаридами происходит декарбоксилиза-ция аминокислот; при этом аминогруппы аминокислот соединяются с альдегидной или кетонной группой моносахаридов. При взаимодействии Сахаров с аминокислотами в качестве промежуточных продуктов образуются фурфурол и оксиметилфурфурол, а также другие побочные вещества. [42]
Как было уже указано, азотистая кислота образует при взаимодействии с аминогруппами аминокислот неустойчивые диазосоединения. Диазогруппы, связанные с ядром тирозина [235, 236] и триптофана, устойчивы. [43]
Фенилаланин-аммиак-лиаза выделена из многих растительных источников [73, 74] в тщательно очищенном виде. Предложен механизм действия фермента [75] ( схема 46), согласно которому аминогруппа аминокислоты Первоначально присоединяется к метиленовой группе дегидроала-нина. [44]
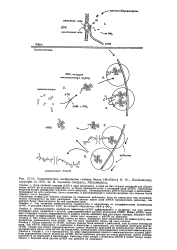 |
Схематическое изображение синтеза белка ( McGilvery, Biochemistry. copyright ( 3 1970, W. B. Saunders Company, Philadelphia. [45] |
Страницы: 1 2 3 4