Осмотический коэффициент
Cтраница 3
Вторые вириальные осмотические коэффициенты были получены [19] из экспериментальных исследований водных растворов диоксида углерода. Интересно отметить, что увеличение температуры приводит к росту отрицательных значений вириальных коэффициентов, т.е. свидетельствует о возрастании притяжения находящихся в воде молекул диоксида углерода друг к другу. [31]
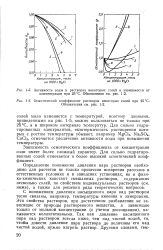 |
Активность воды в растворах некоторых солей в зависимости от концентрации при 25 С. Обозначения 1 - 2.| Осмотический коэффициент растворов некоторых солей при 25 С. Обозначения 1 - 2. [32] |
Зависимость осмотического коэффициента от концентрации соли имеет более сложный характер. Для сильно гидратиро-ванных солей отмечается и более высокий осмотический коэффициент. [33]
Использование осмотических коэффициентов, как это сделал Грегор, не дает удовлетворительных результатов, так как осмотические коэффициенты и коэффициенты активности, как и надо было ожидать, не оказались равноценными. [34]
Смысл осмотических коэффициентов кратко заключается в следующем. В идеальном растворе активность воды aw равна ее молярной доле Nw. В неидеальном растворе рациональный. [35]
Смысл осмотических коэффициентов кратко заключается в следующем. В идеальном растворе активность воды aw равна ее молярной доле Nyf. В неидеальном растворе рациональный. [36]
Следовательно, осмотический коэффициент равен отношению изменения химического потенциала растворителя ( Дщ Hi - ц У) при образовании неидеального раствора сильного электролита данного состава к изменению химического потенциала растворителя при образовании идеального раствора с такой же концентрацией сильного электролита. [37]
Следовательно, осмотический коэффициент равен отношению изменения химического потенциала растворителя ( Ац ц - ц, ) при образовании неидеального раствора сильного электролита данного состава к изменению химического потенциала растворителя при образовании идеального раствора с такой же концентрацией сильного электролита. [38]
Ввиду этого осмотические коэффициенты спиртов, гидроперекисей или аминов в предельных неароматических углеводородах должны быть значительно больше, чем в бензольных растворах. [39]
При пересчете осмотических коэффициентов в коэффициенты активности может возникнуть вопрос, как повлияют на вычисляемые значения lg 7 возможные ошибки в определении значений функции Y по экстраполированной кривой в области малых концентраций. [40]
При гтспользовании осмотического коэффициента ( который, кстати сказать, с ранным основанием можно бтлло бы цалвать также коиффнцш нтпм точки асипенил или точки замерзания) формальное сходство с уравнением для идеальных растворов отчасти теряется, но зато коэффициент ф на много более чувствителен к небольшим отклонениям от неидсалъности, чем коэффициент активности. [41]
Для расчета осмотического коэффициента предлагается [18] использовать уравнение Гиббса - Дюгема с использованием второго приближения Дебая - Гюккеля. [42]
При использовании осмотического коэффициента формальное сходство с уравнением для идеальных растворов отчасти теряется, но зато коэффициент Ф намного больше чувствителен к небольшим отклонениям от идеальности, чем коэффициент активности. [43]
Рассмотрим зависимость осмотического коэффициента от степени диссоциации растворенного вещества. [44]
Из оценки кривых осмотических коэффициентов, упомянутых выше ( рис. 35), для различных смол Глюкауф делает заключение о тесной связи между подвижностью катионов и эффективной молярностью. Различная набухаемость ионообменной смолы является, по Глюкауфу, результатом изменения концентраций свободных ионов в смоле. [45]
Страницы: 1 2 3 4