Вириаль-ной коэффициент
Cтраница 3
Однако метод сравнения рассчитанных и экспериментальных кривых зависимости поверхностного давления от заряда электрода, как было впоследствии отмечено Парсонсом [28], является мало чувствительным к форме изотермы адсорбции. Значительно более чувствительной функцией является дифференциальная емкость электрода. АСд от Е при использовании изотерм адсорбции Генри, Фрейндлиха, Ленгмюра, Темкина и изотермы с вириаль-ными коэффициентами. Сопоставление полученных уравнений с экспериментальными данными по адсорбции на ртути молекул тиомочевины [127] и н - С5НиОН [177] показало, однако, что исследованные изотермы адсорбции лишь в первом приближении могут быть использованы для описания опытных С, Е - кривых. [31]
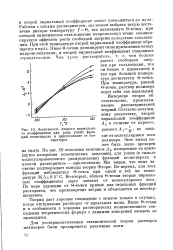 |
Зависимость второго вириально-го коэффициента для ряда узких фракций полистирола в цикпогексане от температуры. [32] |
На рис. 10 отложены величины А 2, измеренные на опыте ( путем измерения осмотических давлений), для узких ( в смысле молекулярновесового распределения) фракций полистирола в плохом растворителе - циклогексане. Мы видим, что опыт частично подтверждает выводы теории Флори. Во-первых, для всех фракций наблюдается 0-точка при одной и той же температуре 34.5 0.5 С. Во-вторых, вблизи в-точки вторые вириаль-ные коэффициенты мало зависят от молекулярного веса. По мере удаления от в-точки кривые для отдельных фракций расходятся, что противоречит теории и объясняется ее несовершенством. [33]
Обсудив природу молекулы воды в идеальном паре, где молекулы не взаимодействуют друг с другом, рассмотрим реальный пар. Свойства реального пара, подобно свойствам льда и жидкой воды, определяются силами, действующими между молекулами. Действительно, исследования воды в парообразном состоянии внесли важный вклад в наши знания о взаимодействиях молекул воды. В этой главе мы рассмотрим сначала происхождение этих сил и их связь со вторым и третьим вириаль-ными коэффициентами пара. Затем подробно обсудим термодинамические свойства реального пара. Мы не будем рассматривать другие свойства пара, такие, как его вязкость и теплопроводность, поскольку эти свойства не являются достаточно полезными для понимания льда, жидкой воды или природы сил, действующих между молекулами воды. [34]
Разделим обсуждение р - v - Т - измерений при высоких давлениях на четыре части. Следует отметить, что в отличие от измерений при низких давлениях при высоких давлениях относительные методы почти не применялись, вероятно, из-за сложности постановки эксперимента. Во второй части этого раздела описываются методы последовательного расширения, а в третьей и четвертой частях - соответственно расчет вириаль-ных коэффициентов из экспериментальных данных и система относительных единиц ( единиц Амага), часто используемых в р - v - Г - измерениях при высоких давлениях. [35]
Первый член в этом выражении есть обычное ван-дер-ваальсовское значение второго вириаль-ного коэффициента и характеризует те взаимодействия между молекулами, которые обусловлены их столкновениями, не приводящими к ассоциации. Второй член характеризует вклад в 32, обусловленный объединением молекул в двойные группы. Как известно, в строгой статистической теории [3] также производится разделение вкладов в ви-риальные коэффициенты соответственно связанным и несвязанным состояниям. Существенное преимущество теории ассоциации состоит в том, что она дает хотя и приближенные, но явные выражения для составляющих вириаль-ных коэффициентов, соответствующих связанным и несвязанным состояниям. [36]
Эти значения определяются методом наименьших квадратов или другим методом подбора выражения для кривой, описывающей экспериментальные данные. Полученные величины Л / ( Т) принимаются непосредственно за вириальные коэффициенты. Следовательно, пока экспериментальные данные не охватывают достаточно низких давлений, функция Ai может не совпадать со вторым вириальным коэффициентом. Поскольку большинство точных измерений сжимаемости газов выполнено при умеренных и высоких давлениях, то из этих измерений трудно получить надежные значения вириаль-ных коэффициентов. Кроме того, коэффициент Аъ ( Т) и последующие коэффициенты весьма чувствительны к показателю степени выбранного полинома; поэтому при вычислении третьего вириального коэффициента по экспериментальным данным приходится сталкиваться с большими трудностями. [37]
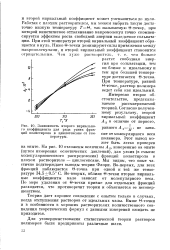 |
Зависимость второго вириально-го коэффициента для ряда узких фракций полистирола в циклогексане от температуры. [38] |
Этот вывод может быть легко проверен на опыте. На рис. 10 отложены величины Аг, измеренные на опыте ( путем измерения осмотических давлений), для узких ( в смысле молекулярновесового распределения) фракций полистирола в плохом растворителе - циклогексане. Мы видим, что опыт частично подтверждает выводы теории Флори. Во-первых, для всех фракций наблюдается 6-точка при одной и той же температуре 34.5 0.5 С. Во-вторых, вблизи В-точки вторые вириаль-ные коэффициенты мало зависят от молекулярного веса. По мере удаления от 0-точки кривые для отдельных фракций расходятся, что противоречит теории и объясняется ее несовершенством. [39]
Страницы: 1 2 3