Орбитальный коэффициент
Cтраница 1
Орбитальные коэффициенты в табл. 25.5 выражены в необычвых единицах ( сДр) 2 / 15, где С - коэффициент, с которым атом 1 или атом 3 входит в данную МО, а Ар - изменение резонансного интеграла при образовании из реагентов переходного состояния ( ср. Величина Др зависит от типа образующейся связи, и для связей С-С, C-N и С-О будет разной. [1]
Рассмотрение орбитальных коэффициентов нафталина показывает, что коэффициенты в соответствующих молекулярных орбиталях, например в X и X, определенным образом связаны друг с другом. Коэффициенты при атомных орбиталях, принадлежащих одному из наборов, имеют в штрихованной ( X) и нештрихованной ( X) МО равные абсолютные величины, но противоположные знаки, в то время как коэффициенты при атомных орбиталях другого набора в обеих МО равны как по абсолютной величине, так и по знаку. [2]
Уравнения для орбитальных коэффициентов имеют вид Ч ( Я. [3]
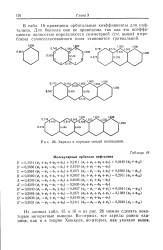 |
Заряды и порядки связей полиаценов.| Молекулярные орбитали нафталина. [4] |
В табл. 16 приведены орбитальные коэффициенты для нафталина. Для бензола они не приведены, так как эти коэффициенты полностью определяются симметрией ( см. выше) и проблема самосогласованного поля становится тривиальной. [5]
Как правило, для вычисления орбитальных коэффициентов приходится решать уравнения МОХ, но несвязывающие МО представляют исключение. [6]
Эта процедура повторяется до тех пор, пока орбитальные энергии и орбитальные коэффициенты не подойдут достаточно близко к пределу, который мы будем считать нашим приближением к истинным решениям уравнений Хартри - Фока. [7]
Когда значения fex и & c - x выбраны, вычисление орбитальных коэффициентов производится, как и раньше. [8]
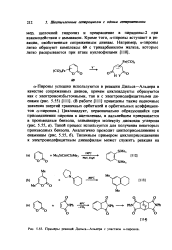 |
Примеры реакций Дильса - Альдера с участием а-пиронов. [9] |
В работе [111] приведены также оценочные значения энергий граничных орбиталей и орбитальных коэффициентов а-пиронов. Такой процесс используется для получения некоторых производных бензола. [10]
Основное достоинство этого метода состоит в том, что мы можем найти орбитальные коэффициенты и энергии МО непосредственно, не прибегая к процедуре самосогласования. Следует отметить, что когда длины связей в молекуле равны, а распределение электронной плотности однородно, хюкке-левские МО совпадают с самосогласованными. Поэтому при рассмотрении молекул, близко удовлетворяющих этим требованиям, часто бывает достаточным ограничиться подстановкой в уравнения Попла (1.5) - (1.7) хюккелевских коэффициентов. Иными словами, в обычном варианте метода Попла собственные векторы аппроксимируются хюккелев-скими ЛКАО - МО. [11]
Дьюар показал, что для альтернантных углеводородов приближенные значения энергий локализации можно легко получить, зная орбитальные коэффициенты несвязы-вятощой МО. Если имеется альтсриаптнкй углеводород RS с четным числом атомов углерода, то его можно представить себе состоящим из двух фрагментов R и S, которые являются нечетными альтернантными углеводородами. [12]
Молекулярные орбитали бензола и пиридина представлены на рис. 2.2. На этих рисунках площади кружочков приблизительно соответствуют относительным орбитальным коэффициентам, а светлые и заштрихованные кружочки показывают противоположные фазы волновых функций. Орбитали пиридина качественно очень похожи на орбитали бензола, но существует два важных отличия. Первое состоит в том, что т-орбитали пиридина имеют более низкую знергию, что обусловлено большей электроотрицательностью атома азота по сравнению с углеродом. Энергии ВЗМО имеют наибольшее значение, потому что, как будет показано в разд. [13]
Если теперь воспользоваться симметрией МО, то можно увидеть, что этих трех уравнений достаточно для определения орбитальных коэффициентов энергий. [14]
Экспериментальные результаты подтверждают этот вывод, что иллюстрируется приведенными ниже примерами, где звездочкой отмечены атомы с наибольшим орбитальным коэффициентом. [15]
Страницы: 1 2 3