Атом - бериллий
Cтраница 1
Атом бериллия под периферийными электронами имеет также оболочку, характерную для наружного энергетического уровня инертного газа, но в отличие от других элементов главной подгруппы это гелиевая оболочка из двух s - электронов. [1]
Атомы бериллия, магния и щелочноземельных металлов в нормальном состоянии имеют нулевую валентность, поскольку у них нет неспаренных электронов. Однако эти элементы можно перевести в возбужденное состояние, в котором внешний электронный слой атомов приобретает конфигурацию ns np - появляются два неспаренных электрона. Для этого надо затратить определенную энергию, закономерно убывающую при переходе от бериллия к барию ( 62 ккал / г-атом для Be, 36 / скал / г-атом для В а) в соответствии с ростом объема атома. Несмотря на то, что энергия, затраченная на возбуждение, велика, при образовании химических соединений происходит выигрыш энергии за счет энергии связи. Поэтому соединения указанных элементов достаточно прочны и в них элементы проявляют степень окисления, равную двум. [2]
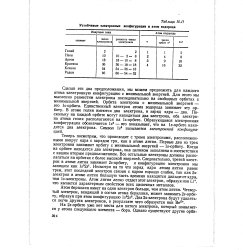 |
Устойчивые электронные конфигурации и атом водорода. [3] |
Атом бериллия имеет на один электрон больше, чем атом лития. [4]
Атом бериллия, так же как и атомы бора и углерода, способен активировать электрон, чтобы он мог участвовать в образовании большего числа химических связей. [5]
Атом бериллия имеет четыре электрона. [6]
 |
Энергетические уровни МО гомоядерной двухатомной молекулы. [7] |
Атом бериллия имеет два валентных электрона, оба на 25-орбитали. В Вб2 только два из четырех валентных электронов могут находиться на МО ( CTI) с более низкой энергией, чем 2s - AO. Два других должны будут занять МО ( 02), которая по отношению к 25-уровню является разрыхляющей. В соответствии с этим бериллий в газообразном состоянии одноатомен, как и гелий. [8]
Атом бериллия состоит из ядра с четырьмя положительными зарядами и из четырех электронов. [9]
Атом бериллия подвергается вр3 ибридизации, поэтому чередующиеся фрагменты структуры лежат в разных плоскостях. Две связи образованы по обменному механизму за счет двух неспаренных электронов атома бериллия ( после промотирования) и двух электронов от двух атомов хлора. Две другие связи осуществляются по донорно-акцепторному механизму за счет двух вакантных 2р - орбиталей бериллия ( акцептор) и двух неподеленных электронных пар атомов хлора. В качестве мос-тиковых функционируют атомы хлора. [10]
Атомы бериллия, не имеющие неспаренных электронов, химически связываться в молекулу Ве2 не должны. [11]
Атом бериллия подвергается р3 - гибридизации, поэтому чередующиеся фрагменты структуры лежат в разных плоскостях. Две связи образованы по обменному механизму за счет двух неспаренных электронов атома бериллия ( после промотирования) и двух электронов от двух атомов хлора. Две другие связи осуществляются по донорно-акцепторному механизму за счет двух вакантных 2р - орбиталей бериллия ( акцептор) и двух неподеленных электронных пар атомов хлора. В качестве мос-тиковых функционируют атомы хлора. [12]
 |
Диаграмма МО для молекулы лития. 6 - 1219. [13] |
Атом бериллия имеет 1 2252-конфигурацию. В молекуле Ве2 таким образом, должно быть четыре валентных электрона, и электронные пары будут занимать и аг и сг2 - орбитали. Как и в случае молекулы Не2, связывающий и разрыхляющий эффекты уравновешиваются. Поэтому устойчивой молекулы Ве2 не существует. [14]
Поэтому атом бериллия способен быть акцептором элек тронных пар и образовывать еще две ковалентные связи по до норно-акцепторному способу. В то же время каждый атом хлора входящий в состав молекулы ВеС12, обладает неподеленными элек тронными парами и может выступать в качестве их донора. [15]
Страницы: 1 2 3 4 5