Атом - бериллий
Cтраница 4
Размеры атома бериллия малы ( атомный диаметр 2 26 А), поэтому атомы примесей сильно искажают решетку и охрупчи-вают его. Чем мельче зерно бериллия, определяемое крупностью исходного порошка, тем выше его прочность и пластичность. [46]
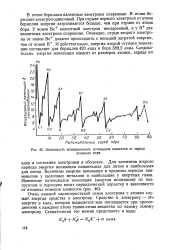 |
Зависимость ионизационного потенциала элементов от заряда. [47] |
В атоме бериллия валентные электроны спаренные. В атоме бора один электрон одиночный. При отрыве первого электрона от атома бериллия энергии затрачивается больше, чем при отрыве от атома бора. У ионов Ве валентный электрон неспаренный, а у В два валентных электрона спаренные. И действительно, энергия второй ступени ионизации составляет для бериллия 420 ккал и бора 589 2 ккал. [48]
В атоме бериллия мы встречаемся с различными состояниями, в которых единичный атом выступает двояко: или как физическое образование - это атом в его нормальном состоянии, или как химический элемент в его возбужденном или валентном состоянии, в котором он находится в соединении с другими атомами. [49]
В атомах бериллия, бора, углерода может происходить разделение электронных пар за счет перехода электронов с 2з - под-уровня на 2р - подуровень, так как в атомах этих элементов на 2р - подуровне имеются вакантные орбитали. Такой переход на более высокий энергетический подуровень внутри данного энергетического уровня не требует больших затрат энергии, может быть скомпенсирован за счет образования химической связи и осуществляется в условиях обычных химических реакций. [50]
 |
Схематическое изображение электронного облака трех р-состояний. [51] |
В атоме бериллия четвертый электрон ( с противоположным спином по отношению к третьему) попадает также на 25-орбиту. [52]
 |
Схематическое изображение электронного облака трех р-орбит. [53] |
В атоме бериллия четвертый электрон ( с противоположным спином по отношению к третьему) попадает также па 2х - орбиту. [54]
 |
Схематическое изображение электронного облака трех р-орбиталей. [55] |
В атоме бериллия четвертый электрон ( с противоположным спином по отношению к третьему) попадает также на 25-орбиталь. [56]
В результате атом бериллия может образовать две связи и делается в возбужденном состоянии двухвалентным. [57]
Ионы и атомы бериллия, как имеющие самые малые размеры ионов и атомов элементов данной подгруппы, образуют наиболее прочную кристаллическую решетку. Поэтому бериллий по твердости, температурам плавления и кипения значительно превосходит остальные элементы главной подгруппы II группы. [58]
Отличие строения атома бериллия от строения атомов магния и щелочноземельных элементов сказывается и на свойствах его соединений. Кроме того, для щелочноземельных металлов и магния характерно образование ионных соединений - тогда как атомы бериллия обычно связаны с атомами других элементов скорее ковалентной связью, чем ионной. [59]
Отличие строения атома бериллия от строения атомов магния и щелочноземельных элементов сказывается и на свойствах его соединений. Кроме того, для щелочноземельных металлов и магния характерно образование ионных соединений, тогда как атомы бериллия обычно связаны с атомами других элементов скорее ковалентной связью, чем ионной. [60]
Страницы: 1 2 3 4 5