Атом - бериллий
Cтраница 3
 |
Схема строения линейного полимера черные кружки - атомы бериллия. белые - атомы хлора. [31] |
Здесь атом бериллия находится в состоянии 5 /) 3-гибридизации, благодаря чему ион ВерГ построен в форме тетраэдра. Тетра-эдрическое расположение атомов бериллия и кислорода характерно и для кристаллического оксида бериллия. [32]
Каждый атом бериллия в хлориде связан с четырьмя атомами хлора, а каждый атом хлора - с двумя атомами бериллия. [33]
Каждый атом бериллия вносит в твердое тело четыре электрона. Два из них поступают с ls - орбитали атома; их достаточно, чтобы полностью заполнить ls - зону. Два других поступают с 25-орбитали, они полностью заполняют 25-зону. [34]
Поэтому атом бериллия способен быть акцептором электронных пар и образовывать еще две ковалентные связи по до-норно-акцепторному способу. В то же время каждый атом хлора, входящий в состав молекулы ВеС12, обладает неподеленными электронными парами и может выступать в качестве их донора. [35]
 |
Схема строения линейного полимера ( ВеС1. [36] |
Здесь атом бериллия находится в состоянии р3 - гибридизации, благодаря чему ион ВеРГ построен в форме тетраэдра. Тетра-эдрическое расположение атомов бериллия и кислорода характерно и для кристаллического оксида бериллия. [37]
У атома бериллия этот подуровень заполнен и нет ни одного неспаренного электрона, следовательно, бериллий не должен образовывать ни одной химической связи. У бора и следующих за ним элементов ( С, N, О, F) происходит последовательное заполнение 2 / - подуровня, и атомы этих элементов будут иметь определенное число неспаренных электронов. Если при образовании связей учитывать только наличие неспаренных электронов, то для этих элементов должны образоваться следующие водородные соединения: ВН, СН2, NH3, Н2Э, HF. Устранить это противоречие можно, предположив, что атомы элементов второго периода в образовании молекул участвуют в возбужденном состоянии, т.е. происходит распаривание - электронов и переход их на - подуровень. Но тут возникает другое несоответствие с опытными данными. Согласовать теорию и эксперимент можно, введя предположение об усреднении энергий s - и - подуровней и образовании новых уровней, на которых энергии электронов, находящихся уже на орбиталях другого типа, одинаковы. А раз это так, то по правилу Хунда, в атоме появляется максимальное число неспаренных электронов. Эта гипотеза получила название явления гибридизации, а орбитали, образующиеся в результате усреднения энергий подуровней, называются гибридными. Естественно, что при этом меняются и форма электронных облаков, и их расположение в пространстве. Число получившихся гибридных орбиталей должно быть равно общему числу орбиталей, вступивших в гибридизацию. [38]
 |
Карты зарядовых плотностей в сечениях кластеров, моделирующих примесные системы Si2N2O. M ( М С, Al, Be, Mg. Расчет методом дискретного. [39] |
Для атомов бериллия и магния характер их взаимодействия с матрицей весьма различен. [40]
Энергия атома бериллия ( энергия присоединения четырех электронов к ядру бериллия), как показывает вычисление, близка к 14 67 ат. Энергия атома кислорода составляет около 75 07 ат. В сумме энергия исходных свободных атомов равна 56 339 ккал. Энергия образования ( ВеО) из атомов, экспериментально найденная, равна всего лишь 106 ккал / моль или 0 165 ат. Необходимо достоверно знать пять значащих цифр. При переходе к более многоэлектронным атомам число знаков, за которые надо ручаться, быстро растет. [41]
 |
Направление валентности в молекуле бутана. [42] |
Для атомов бериллия ( 0-валентный), бора ( одновалентный) и углерода ( двухвалентный), находящихся-в нормальном ( основном) состоянии, эта схема дает неправильные значения. [43]
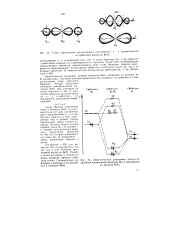 |
Схема образования трехцентровой связывающей т - и разрыхляющей. [44] |
У атома бериллия 2рл - и 2р - орбитали с орбиталями водорода не комбинируются и в молекуле играют роль несвязывающих одноцентровых орбиталей, принадлежащих лишь атому бериллия. Энергия электронов на несвязывающих молекулярных орбиталях практически такая же, как и на атомных орбиталях. В символах метода молекулярных орбиталей 2р - и 2р обозначают л - МО. [45]
Страницы: 1 2 3 4 5