Атом - бор
Cтраница 1
Атомы бора связаны с алюминием водородными мостиками. Эта система характеризуется дефицитом электронов и может рассматриваться с позиции теории трехцентровых связей. [1]
Атом бора имеет три валентных электрона и четыре валентные орбитали. Углерод имеет четыре валентных электрона и четыре орбитали. За исключением тех случаев, когда он образует кратные связи, эти орбитали используются для 5р3 - гибридизации. Атом азота имеет пять валентных электронов и четыре орбитали. Как правило, он образует три связи с другими атомами в структурах с тетраэд-рической конфигурацией, а четвертая гибридная хр3 - орбиталь у него занята неподеленной электронной парой ( разд. Углерод и азот способны образовывать двойные и тройные связи в результате я-перекры-вания, обсуждавшегося в разд. Прочность кратной связи повышается благодаря наличию электронов на связывающей молекулярной я-орбитали, возникающей в результате перекрывания атомных я-ор-биталей. Но перекрывание я-типа между орбиталями становится достаточно большим для возникновения связи только при близком расположении атомов. По этой причине Si и другие элементы третьего и следующих периодов неспособны образовывать кратные связи. Кремний имеет 10 внутренних электронов по сравнению с 2 в атомах С и N. Отталкивание этих внутренних электронов не позволяет двум атомам Si сблизиться настолько, насколько это необходимо для достаточного я-перекрывания р-орбиталей и возникновения двойных связей. [2]
Атом бора в борине электронно ненасыщен, так как его внешняя оболочка не заполнена до октета. Пара электронов гидрид-иона Н - гидрида лития, поэтому, становится общей для центрального атома бора и гидрид-иона. В результате возникает комплексный ион ВШ, в котором все ковалентные связи водород-бор, равноценны. Гидрид-анион BHI и катион Li образуют ионную связь. [3]
Атомы бора и углерода располагаются по вершинам многогранника, грани которого являются треугольниками. [4]
Атом бора в триэтилборате имеет незавершенную электронную оболочку ( 6 электронов вместо 8), поэтому он легко присоединяет атомы, имеющие неподеленную электронную пару. В частности, он легко присоединяет еще одну молекулу этилового спирта за счет неподеленной пары электронов кислорода. [5]
Атом бора имеет одну свободную валентность 2р - электрона, в невозбужденном состоянии, атом алюминия - одну свободную валентность Зр-электрона, а атом азота - три свободные валентности 2р - электронов. Однако в соединениях атомы бора и алюминия, как правило, трехвалентны. Это происходит вследствие одноэлек-тронного перехода 2s - 2р в боре, обусловливающего р2 - конфигу-рацию и одноэлектронного перехода 3s - Зр в алюминии, также способствующего образованию / - конфигурации. Три связи, образуемые тремя валентностями азота и тремя валентностями возбужденных атомов бора осуществляются в базисной плоскости нитрида бора. Связь между базисными плоскостями осуществляется вследствие несимметричности поля, в котором находятся валентные электроны атомов бора и азота. [6]
Атом бора имеет четыре орбитали в валентной оболочке и три валентных электрона. [7]
Атомы бора в молекуле В2 валентно и координационно ненасыщены. Поэтому при конденсации паров возможно образование новых химических связей - происходит процесс полимеризации. [8]
Атом бора - конструкция довольно простая. Вокруг ядра вращаются пять электронов: два - на ближайшей к ядру оболочке, три - на наружной. [9]
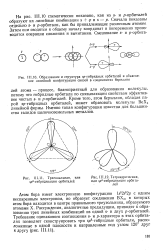 |
Образование и структура sp - гибридных орбиталей и объяснение линейной конфигурации связей в соединениях бериллия.| Тетраэдрическая, или 5р3 - гибридизация орбита. [10] |
Атом бора имеет электронную конфигурацию Is22s22p с одним неспаренным электроном, но образует соединения ВХ3, в которых атом бора находится в центре правильного треугольника, образуемого атомами X. Рассуждения, аналогичные предыдущим, приводят к образованию трех линейных комбинаций из одной s - и двух р-орбиталей. [11]
Атомы бора образуют сетки, аналогичные сеткам атомов углерода в графите и располагающиеся между двумя перпендикулярными оси С плоскостями атомов алюминия так, что атомы алюминия находятся в центре шестигранных призм, составленных из атомов бора. [12]
 |
Тетраэдрическая структура соединения углерода. яр3 - связь.| Структура BF3. зр - - связь. [13] |
Атом бора в молекуле BF3 использует для образования связей одну 2з - орбиту и две 2 / ьорбиты. [14]
Атом бора имеет 3 валентных электрона и в ряде своих соединений образует 3 компланарные связи, направленные к вершинам равностороннего треугольника, что соответствует sp2 гибридизации. Это валентное состояние проявляется в галогенидах бора состава ВНа13, четырехатомные молекулы которых имеют форму правильного треугольника. [15]
Страницы: 1 2 3 4 5