Атом - халькоген
Cтраница 2
Уменьшение резонансного эффекта групп СНгСНХ по сравнению с СН3СН2Х вызвано конкурирующим р - я-сопряжением атомов халькогена ( X) с двойной связью: по мере ослабления этого взаимодействия в ряду О S Se Те различия между значениями OH групп - СН2СНХ и СН3СН2Х исчезают. Положительные значения констант OH при X SO и S02 свидетельствуют о преимущественно л-акцепторном характере взаимодействия этих групп с ненасыщенным фрагмент ом, величина которого мало зависит от характера второго заместителя. [16]
Уменьшение резонансного эффекта групп СНгСНХ по сравнению с СН3СН2Х вызвано конкурирующим р - я-сопряжением атомов халькогена ( X) с двойной связью: по мере ослабления этого взаимодействия в ряду 0S Se Те различия между значениями OH групп - СН2СНХ и СН3СН2Х исчезают. Положительные значения констант OH при X SO и S02 свидетельствуют о преимущественно л-акдепторном характере взаимодействия этих групп с ненасыщенным фрагмент ом, величина которого мало зависит от характера второго заместителя. [17]
При использовании двух наружных наполовину занятых р-орбиталей атомы могут образовать две простые ковалентные связи, причем атом халькогена обычно заряжен отрицательно. [18]
Для халькогенидов d - переходных металлов характерно наложение нескольких типов химической связи; ковалентной - между атомами халькогенов, металлической и ионной - между атомами металлов, с одной стороны, и атомами или группами атомов халькогена, с другой. [19]
 |
Структура 5 % и D. [20] |
В основе всех предложенных структур ( для описания фаз типа А2В2С4) лежит почти кубическая плотнейшая упаковка атомов халькогенов, в тетраэдрических пустотах которой распределены металлические атомы в соответствии с пространственными группами, приписываемыми данным фазам. [21]
В случае GeY2 структура исследована с помощью комбинационного рассеяния света [5.104-5.107] и других методов [5.108, 5,109] и представляет собой атомы Ge с координационным числом четыре и атомы халькогенов с координационным числом два, расположенные в тетраэдрах GeY - t, причем атомы Y соединяют тетраэдры между собой. [22]
Для халькогенидов d - переходных металлов характерно наложение нескольких типов химической связи; ковалентной - между атомами халькогенов, металлической и ионной - между атомами металлов, с одной стороны, и атомами или группами атомов халькогена, с другой. [23]
Чтобы показать, как ковалентность модифицирует электронную структуру по сравнению с ионным пределом модели Рот, мы приводим на рис. 8.6 ту же последовательность для случая, когда связь М - А частично ковалентна, а А - атом халькогена. [24]
У молекул воды угол между связями О - Н равен 104 5 ( sp - гибридизация АО кислорода), а в остальных халькогеноводородах этот угол близок к 90, что свидетельствует об отсутствии гибридизации s - и р - АО атомов халькогенов и участии в образовании связей чистых р - АО. [25]
Между атомами металла и халькогена существует прочная химическая связь, в между атомами халькогена эта связь слабая. Поэтому в направлении связей между атомами халькогена происходит сдвиг с небольшим трением, что обеспечивает высокие смазочные свойства WSe2 NbSe2, TaSe2 и других соединений. [26]
Авторы рассматривают последнюю как кубически плотно упакованную решетку атомов халькогена, в тетраэдрических пустотах которой упорядоченно размещены атомы металла. [27]
Важной особенностью рассматриваемой схемы является то, что число состояний в каждой зоне определяется числом атомов и связей. Ясно, что для любой молекулярной системы с полностью насыщенными ковалент-ными связями, содержащей атомы халькогенов, уровень Ферми располагается выше зон, образованных электронами атомов халькогенов, не участвующих в образовании связей. [28]
Наибольшее распространение имеют нормальные халькогениды, в которых атомы металла непосредственно соединены лишь с атомами халькогена. [29]
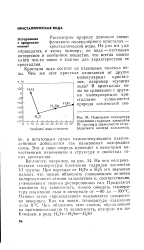 |
Изменение температур плавления гидридов элементов VI группы в зависимости от порядкового номера халькогена. [30] |
Страницы: 1 2 3