Атом - хлор
Cтраница 2
Атом хлора в DM вступает а различные реакции обмена н в неводной среде замещается другими атомами или функциональными группами. [16]
Атомы хлора, находящиеся в орто - и параположениях к аминогруппе, сильно ослабляют основные свойства аминов, но хлор в ме-таположении оказывает лишь незначительное влияние на основность амина. [17]
Атомы хлора в нем связаны чрезвычайно прочно и не омыляются даже горячим раствором едкого натра. Лишь при нагревании с твердым NaOH - отщепляется хлористый водород, но также лишь с большим трудом. Наоборот, этот эфир легко вступает в реакцию с различными алко-голятами и аминами 9, чем весьма напоминает свойства своего сернистого аналога - иприта. Тем более загадочно отсутствие у [ ifi1 - дихлордиэтилового эфира кожного действия. [18]
Атомы хлора в хлористом сульфуриле, как и вообще в хлор-ангидридах, связаны сравнительно непрочно. [19]
Атом хлора в радикале, как находящийся при двойной связи, весьма мало реакционноспособен и при ряде реакций-окислении и осторожном гидролизе - не затрагивается. [20]
Атом хлора гораздо менее активен, чем атом фтора, и только одна из стадий процесса хлорирования более экзотермична. [21]
Атом хлора в положениях 5 и 6 бензофуроксана сильно повышает реакционную способность по отношению к еиаминам, ио в положениях 4 и 7, как н другие заместители, резко замедляет реакцию, видимо, из-за пространственных затруднений, вызванных взаимным отталкиванием этих заместителей и N-оксндных групп в конечном продукте. [22]
Атом хлора, ие очень отличаясь по размерам от метальной группы, в то же время оказывает противоположное электронное влияние, и поэтому при замене 6 - Ме на 6 - С1 скорость термолиза возрастает. [23]
Атомы хлора в побочно образующемся кетоне не находятся под непосредственным активирующим влиянием ненасыщенной системы, как у соединений типа бензальхлорида, чем и объясняется устойчивость этого кетона в щелочной среде. [24]
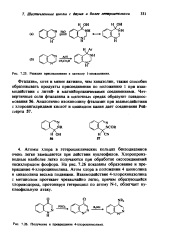 |
Реакции присоединения к катиону 1-хииазолииия.| Получение и превращение 4-хлороциииолииа. [25] |
Атомы хлора в гетероциклических кольцах бензодиазинов очень легко замешаются при действии нуклеофилов. Хлоропроиз-водные наиболее легко получаются при обработке оксосоединений оксихлоридом фосфора. На рис. 7.26 показаны образование и превращение 4-хлороциннолина. Атом хлора в положении 4 циннолина и хиназолина весьма подвижен. Взаимодействие 4-хлорохиназолина с метанолом протекает чрезвычайно легко, причем образующийся хлороводород, протонируя гетероцикл по атому N-1, облегчает ну-клеофильную атаку. [26]
Атом хлора в 1-хлор - 2 4-динитробензоле очень подвижен, поэтому соединение это используется как исходный материал для получения 2 4-динитрофенола, 2 4-динитроанилина и 2 4-динитродифениламина. [27]
Атом хлора в хлорангидридах кислот отличается большой подвижностью; поэтому хлорангидриды находят широкое применение при различных синтезах, В частности, хлорангидриды ароматических кислот часто используются для выделения и идентификации спиртов, а также первичных и вторичных аминов, с которыми они образуют ацильные производные, в большинстве случаев мало растворимые и хорошо кристаллизующиеся. [28]
Атомы хлора имеют плотно упакованное расположение с ромбоэдрической симметрией. Каждая пара атомов алюминия окружена шестью атомами хлора, образуя отдельные группы в виде АЬСЦ. Хлорид алюминия возгоняется при 182 7 С и плавится при 192 4 С и давлении 2 5 - Ю5 Па. Давление его паров при 180 2 С равно 105 Па. Он хорошо растворим в воде и почти во всех органических растворителях. [29]
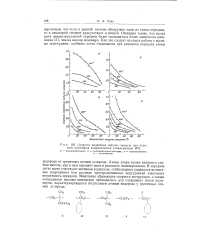 |
Скорость выделения летучих веществ при пиролизе полимеров алифатических углеводородов. [30] |
Страницы: 1 2 3 4