Атом - элемент - период
Cтраница 2
Предельный хартри-фоковский базисный набор даже для атомов элементов II периода включает все АО вплоть до вакантных в основном состоянии этих атомов 3d - и 4 / - орбиталей. [16]
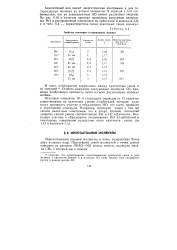
В табл. 16 показаны электронные схемы атомов элементов I-IV периодов. [17]
 |
Свойства некоторых гетероядерных молекул. [18] |
Аналогичный вид имеют энергетические диаграммы и для ге-тероядерных молекул из атомов элементов II периода с той особенностью, что их эквивалентные АО имеют различную энергию. На рис. 6.16 в качестве примера приведены контурные диаграммы МО и распределение электронов по орбиталям в молекуле СО, а в табл. 6.4 - характеристики связи некоторых таких молекул. [19]
Представленная на рис. 6.15 энергетическая диаграмма характеризует электронное строение всех гомоядерных молекул, образованных атомами элементов II периода. [20]
Количество энергетических уровней соответствует номеру периода, в котором находится элемент. Атомы элементов I периода имеют один энергетический уровень. [21]
Высшим пределом может быть такое значение валентности, которое равно числу возможных орбиталей на внешнем уровне атома. У атомов элементов II периода, куда входит и азот, на внешнем уровне имеется четыре орбитали: одна s - и три р-орбитали. А значит, максимальное значение ковалентных связей ( в том числе и образованных по донорно-акцепторному механизму) равно четырем. И валентность азота равна четырем. [22]
Высшим пределом может быть такое значение валентности, которое равно числу возможных орбиталей на внешнем уровне атома. У атомов элементов II периода, куда входит и азот, на внешнем уровне имеется четыре орбитали: одна s - и три / о-орбитали. А значит, максимальное значение ковалентных связей ( в том числе и образованных по донорно-акцепторному механизму) равно четырем. И валентность азота равна четырем. [23]
Высшим пределом валентности может быть такое значение, которое равно числу возможных орбиталей на внешнем уровне атома. У атомов элементов II периода, куда входит и азот, на внешнем уровне имеется четыре орбитали: одна 5 - и три р-орбитали. А значит, максимальное значение ковалентных связей ( в том числе и образованных по донорно-акцепторному механизму) равно четырем. И валентность азота равна четырем. [24]
 |
Соотношение между энергиями стабилизации монозамещенных метил-катионов и о - константами заместителей. [25] |
Как видно из рис. IV-2, имеется очень хорошая корреляция между значениями относительной энергии стабилизации катионов и значениями а - констант заместителей, имеющих атомы элементов второго периода. Заместители, имеющие атомы элементов более высоких периодов, выпадают из корреляции. По-видимому, их высокая способность стабилизировать катион в газообразном состоянии обусловлена их большей поляризуемостью. [26]
Таким образом, максимальная ковалентность атомов элементов II периода равна четырем. Максимальная ковалентность атомов элементов III периода равна шести, что соответствует участию в образовании связей одной 3s -, трех Зр - и двух Sd-орбиталей. [27]
 |
Полосы поглощения некоторых силанов. [28] |
Тем не менее учитывать роль атомов элементов высших периодов, в особенности серы, фосфора и кремния, в построении электронных систем молекул органических соединений необходимо. [29]
Приведенные выше данные указывают на то, что в структурах соединений-аналогов типа AIVBV, AraBVI, Ап Bvn атомы имеют тетраэдрическую, октаэдрическую и тригонально-пирамидальную координацию и, следовательно, смешанную ионно-ковалентную природу связи, изменяющуюся в зависимости от электронной структуры атомов, входящих в состав соединений. При этом у соединений с атомами элементов нижних периодов периодической системы ( Sn, Hg, Tl, Sb) нарастает доля металлической связи и в рядах аналогов свойства изменяются от ионных до металлических. [30]
Страницы: 1 2 3