Атом - элемент - побочная подгруппа
Cтраница 2
Отличие в строении атомов элементов побочной подгруппы от главной состоит в том, что на предвнешнем энергетическом уровне атомы имеют кроме s - и р - еще и ( i-электроны. Элементы под-группы меди в соединениях проявляют не только степень окисления 1, но и более высокие степени окисления за счет - электронов предвнешнего уровня. Способность атомов меди и золота отдавать два и три электрона объясняется тем, что орбита ли 3d и 4s у меди, 5d и 6s у золота близки по энергиям. [16]
 |
Некоторые свойства атомов элементов подгруппы меди. [17] |
Отличие в строении атомов элементов побочной подгруппы от главной состоит в том, что на предвнешнем энергетическом уровне атомы имеют кроме s - и р - еще и cf - электроны. В связи с этим элементы подгруппы меди в соединениях проявляют не только степень окисления 1, но и более высокие степени окисления. Способность атомов меди и золота отдавать два и три электрона объясняется тем, что орбитали 3d и 4s меди, 5d и 6s золота близки по энергиям. [18]
Подобно атомам щелочных металлов атомы элементов побочной подгруппы I группы, или подгруппы меди, содержат на s - подуровне внешнего квантового слоя по одному электрону. [19]
Чем отличается электронное строение атомов элементов побочной подгруппы IV группы от электронного строения атомов элементов главной подгруппы IV группы. Как это сказывается на их свой -, ствах. [20]
Таким образом, наружные электроны у атомов элементов побочной подгруппы находятся значительно ближе к ядру и, следовательно, прочнее удерживаются ядром. Поэтому в отличие от щелочных металлов элементы подгруппы меди являются одними из наименее активных металлов. В ряду напряжений эти металлы стоят после водорода и занимают последние места. [21]
В чем проявляется сходство в строении атомов элементов побочных подгрупп I и II группы периодической системы и отличие их от элементов главных подгрупп тех же групп. [22]
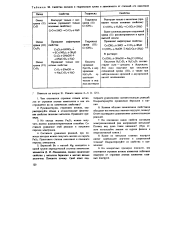 |
Свойства оксидов и гидроксидов хрома в зависимости от степеней его окисления. [23] |
На конкретных примерах поясните, чем отличается строение атомов элементов побочных подгрупп от строения атомов элементов главных подгрупп. [24]
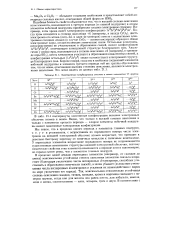 |
Электронные конфигурации атомов и ионов элементов VI группы. [25] |
Подобная близость свойств объясняется тем, что в высшей степени окисления атом элемента, находящегося в третьем периоде ( в главной подгруппе) и атомы элементов побочной подгруппы приобретают сходное электронное строение. Когда хром находится в степени окисления 6 ( например, в оксиде СгОз), шесть электронов его атома ( пять 3d - и один 4з - электрон) вместе с валентными электронами соседних атомов ( в случае СгОз - атомов кислорода) образуют общие электронные пары, осуществляющие химические связи. Остальные электроны, непосредственно не участвующие в образовании связей, имеют конфигурацию Is22s p63s2p6, отвечающую электронной структуре благородного газа. Аналогично у атома серы, находящегося в степени окисления 6 ( например, в триокси-де серы 80з), шесть электронов участвуют в образовании ковалентных связей, а конфигурация остальных ( Is22s2p6) также соответствует электронной структуре благородного газа. Короче говоря, сходство в свойствах соединений элементов побочной подгруппы и элемента третьего периода той же группы обусловлено тем, что их ионы, отвечающие высшим степеням окисления, являются электронными аналогами. [26]
Элементы главных и побочных подгрупп отличаются характером заполняемых орбиталей. В атомах элементов побочных подгрупп идет заполнение ( п - ) d - или ( п - 2) / - орбиталей, где п-главное квантовое число, которое определяет число электронных слоев в атоме любого элемента. Основное отличие элементов побочных подгрупп ( d - и / - элементов) от элементов главных подгрупп состоит в том, что в атомах этих элементов заполняется не внешний электронный слой, а предшествующие ему, причем заполнение d - орбиталей опаздывает на один период, а / - орбиталь заполняется с опозданием на два периода. [27]
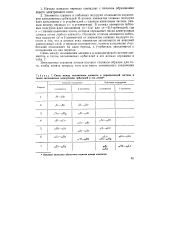 |
Связь между положением элемента в периодической системе и типом заполняемых электронами орбиталей в его атоме. [28] |
Элементы главных и побочных подгрупп отличаются характером заполняемых орбиталей. В атомах элементов побочных подгрупп идет заполнение ( п - l) d - или ( п - 2) / - орбиталей, где п - главное квантовое число, которое определяет число электронных слоев в атоме любого элемента. Основное отличие элементов побочных подгрупп ( d - и f - элементов) от элементов главных подгрупп состоит в том, что в атомах этих элементов заполняется не внешний электронный слой, а предшествующие ему, причем заполнение d - op - биталей опаздывает на один период, а f - орбиталь заполняется с опозданием на два периода. [29]
Число валентных электронов атома соответствует номеру группы, в которой находится элемент в периодической системе. У атомов элементов главных подгрупп все валентные электроны расположены в наружном слое; у атомов элементов побочных подгрупп и 8 - й группы часть валентных электронов находится в более глубоком электронном слое. Марганец тоже находится в седьмой группе, но в побочной подгруппе, наибольшая валентность марганца по кислороду тоже равна семи и соответствует номеру группы; но семь валентных электронов марганца находятся в двух слоях: два электрона в наружном слое и пять электронов в более глубоком. [30]
Страницы: 1 2 3