Атом - элемент - второе - период
Cтраница 4
В соответствии с методом ВС валентность атома равна числу его одиночных электронов. В этой позиции валентности атомов элементов второго периода системы элементов Д. И. Менделеева объясняют следующим образом. Первый энергетический уровень заполнен ( Is2) и не может внести вклад в валентность атома. [46]
 |
Схематическое изображение рл - rf - трисилиламине. [47] |
Вакантные d - орбитали атомов элементов третьего периода также могут перекрываться со связывающими п-орбиталями кратных связей или р-орбиталями неподеленных электронных пар. Эти связи отличаются по свойствам от обычных связей между атомами элементов второго периода. [48]
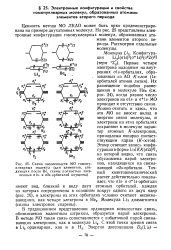 |
Схема заселенности МО гомонуклеарных молекул ( для элементов, следующих после Be, схемы полностью заселенных als - и 025-орбиталей опущены. [49] |
Ценность метода МО ЛКАО может быть ярко продемонстрирована на примере двухатомных молекул. На рис. 25 представлены электронные конфигурации гомонуклеарных молекул, образованных атомами элементов второго периода. [50]
В соответствии с этими представлениями при образовании молекул из атомов второго периода происходит заполнение внешней электронной оболочки с образованием восьмиэлектронной системы, состоящей из четырех электронных пар, которые могут образовывать ковалентные связи или находиться в виде неподеленных пар электронов. С точки зрения современных представлений правило октета может быть объяснено следующим образом: у атомов элементов второго периода имеются четыре орбитали ( одна 25-орби-таль и три 2р - орбитали), способные принимать участие в образовании химических связей. Зр-орбитали находятся значительно выше по энергии и не принимают существенного участия в связывании. Поэтому атомы элементов второго периода не могут образовывать больше четырех ковалентных связей, причем наиболее энергетически выгодное состояние достигается ари наличии у каждого атома восьмиэлектронной оболочки. [51]
Как и в случае F и С1, это можно прежде всего объяснить меньшими размерами атомов элементов второго периода, что приводит к очень высокой электронной плотности в соответствующих отрицательных ионах. Высокая электронная плотность увеличивает энергию межэлектронного отталкивания. [52]
Большая часть частиц этого типа, являющихся моноокисями или моногалогенидами металлов, рассмотрена в гл. Что касается исследованных в матрице молекул, не содержащих атомов металлов, то они состоят в основном из атомов элементов второго периода. [53]
Страницы: 1 2 3 4