Атом - переходный элемент
Cтраница 1
Атомы переходных элементов обладают, таким образом, переменной валентностью. [1]
Атомы переходных элементов способны, следовательно, поглощать малые кванты энергии. Это приводит к тому, что переходные элементы поглощают ( и испускают) свет в видимой части спектра. Поглощение в видимой части спектра означает наличие цвета у тела как в отраженном, так и в проходящем свете. [2]
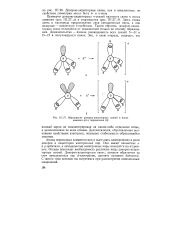 |
Образование донорно-акцепторных связей в ионах аммония ( а и гидроксония ( б. [3] |
Атомы переходных элементов могут выступать одновременно в роли доноров и акцепторов электронных пар. Они имеют вакантные s - и р-орбитали, а неподеленные электронные пары находятся на d - уров-нях. Отсюда возникает необходимость различать виды донорно-акцепторных связей. Донорно-акцепторную связь, которая образуется за счет неподеленных пар d - электрбнов, принято называть дативной. [4]
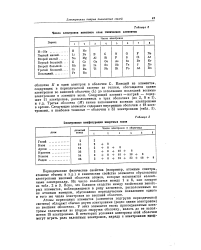 |
Число электронов внешнего слоя типических элементов. [5] |
Атомы переходных элементов ( элементов подгрупп периодической системы) обладают обычно двумя электронами ( редко одним электроном) во внешних оболочках. У этих элементов вновь присоединяемые электроны включаются во вторую снаружи оболочку, вплоть до ее заполнения 18 электронами. [6]
Атомы переходных элементов используют при образовании связей не только валентные 5 - и / мэрбитали, но и близко расположенные rf - орбитали. Тем не менее существуют глубокие аналогии в характере связывания металлоорганических и чисто органических фрагментов, обусловленные сходной формой тех орбиталей этих фрагментов, взаимодействие которых определяет природу связывания. [7]
Атомы переходных элементов способны, следовательно, поглощать малые кванты энергии. Это приводит к тому, что переходные элементы поглощают ( и испускают) свет в видимой части спектра. Поглощение в видимой части спектра означает наличие цвета у тела как в отраженном, так и в проходящем свете. [8]
Атомы переходных элементов используют при образовании связей не только валентные 5 - и / мэрбитали, но и близко расположенные rf - орбитали. Тем не менее существуют глубокие аналогии в характере связывания металлоорганических и чисто органических фрагментов, обусловленные сходной формой тех орбиталей этих фрагментов, взаимодействие которых определяет природу связывания. [9]
 |
Пространственная конфигурация гибридных связей в молекуле. [10] |
Атомы переходных элементов в валентном состоянии содержат наряду с s - и р - также и d - электроны. [11]
Атомы переходных элементов могут вступать в реакцию как с самим кремнием, так и с его оксидом, образуя ряд силицидов. [12]
Атомы переходных элементов могут выступать одновременно в роли доноров и акцепторов электронных пар. Они имеют вакантные s - и р-орбитали, а неподеленные электронные пары находятся на d - уров-нях. Отсюда возникает необходимость различать виды донорно-акцепторных связей. Донорно-акцепторную связь, которая образуется за счет неподеленных пар d - электронов, принято называть дативной. [13]
Для атомов переходных элементов отмечаются две тенденции, определяющие в конечном итоге их химические свойства. С одной стороны, заполняющиеся внутренние d - или / - оболочки по мере увеличения электронов в них способствуют экранированию внешних / zs - электронов, в силу чего их связь с ядром должна ослабляться. Но, с другой стороны, рост числа электронов на внутренних уровнях приводит к уменьшению атомного радиуса. Наиболее ярко это явление выражено у лантаноидов и получило, как известно, название лантаноидной контракции. В результате контракции связь внешних электронов с ядром должна усиливаться. Наложение этих двух противоположных тенденций приводит к тому, что хотя d - и / - элементы обладают металлическими свойствами, эти свойства выражены у них менее ярко, чем у s - и / - металлов. [14]
Для атомов переходных элементов отмечаются две тенденции, определяющие в конечном итоге их химические свойства. С одной стороны, заполняющиеся внутренние d - или / юрбитали по мере увеличения в них числа электронов способствуют экранированию внешних я-электронов в силу чего их связь с ядром должна ослабляться. Но, с другой стороны, рост числа электронов на внутренних уровнях приводит к уменьшению атомного радиуса. Наиболее ярко это явление выражено у лантаноидов и получило, как известно, название лантаноидной контракции. В результате контракции связь внешних электронов с ядром должна усиливаться. [15]
Страницы: 1 2 3 4