Атом - переходный элемент
Cтраница 3
Как известно, структура атомов переходных элементов различается зарядом ядра, числом d - электронов и внешних s - электро-нов. Последние имеют сравнительно малое значение из-за преимущественного образования благородными металлами комплексных соединений и малого числа простых солей. [31]
На внешней электронной оболочке атомов переходных элементов содержатся два, иногда один и даже нуль ( у палладия) электронов. Поэтому переходные элементы в образуемых ими соединениях имеют положительную степень окисления и выступают в качестве характерных металлов, проявляя тем самым сходство с металлами главных подгрупп. [32]
Специфика структуры электронных оболочек атомов переходных элементов ( d - и / - элементов) давно привлекает внимание химиков и физиков. Было доказано, что у d - элементов уровни энергии ( п -) d -, ns -, np - орбита-лей лежат близко один к другому, поэтому у них имеет место конкуренция между d - и s - электронами. Наиболее отчетливо это проявляется для d - под-уровня при заполнении его наполовину и особенно при окончании заполнения. [33]
При наличии в веществе атомов переходных элементов, у которых имеются незаполненные внутренние оболочки. [34]
Следствием такой близости размеров и строения атомов переходных элементов является способность к образованию твердых растворов между ними, что широко используется в технике для создания огромного числа разнообразных сплавов. [35]
Наблюдающиеся в действительности рентгеновские Кос1 2-ли-нии атомов переходных элементов представляют собой результат наложения слегка смещенных друг относительно друга двух или большего числа линий спин-дублета. Эти линии появляются вследствие электронных переходов в атомах этих элементов, находящихся в различных валентных состояниях, соответствующих, например, различным окислам этих элементов в пределах единого испытуемого образца. Нетрудно поэтому понять, какое влияние будет оказывать на дублетное расстояние частичное восстановление или дальнейшее окисление вещества в процессе эксперимента. Такое воздействие должно будет неизбежно приводить к перемещению центра тяжести линий ( грубо говоря, их максимума) в сторону того компонента суммарной кривой, интенсивность которого растет в процессе частичного восстановления или окисления вещества. При этом, из-за неодинаковости взаимных смещений - компонентов в пределах каждой из линий Ка Дублета, в одном случае может наблюдаться кажущийся рост дублетного расстояния, а в другом - его уменьшение. Степень чувствительности Ка - ли-ний различных элементов группы железа к внешним воздействиям, способным изменять валентное состояние элемента, должна быть, естественно, тем значительнее, чем большую склонность к образованию устойчивых разновалентных окислов проявляет элемент ( марганец, железо в опытах Красникова) и чем дальше отстоят друг от друга соответствующие этим окислам компоненты суммарной линии испускания. С этой точки зрения не вызывают никаких недоумений и наблюдавшиеся Красниковым колебания в ширине соответствующих линий испускания. Ширина суммарной линии испускания, измеряемая экспериментально, не является, невидимому, для этой группы элементов истинной шириной индивидуальной спектральной линии и может весьма сильно изменяться вследствие выпадания большего или меньшего числа компонентов линии, зависящего от степени химической ( в рассматриваемом смысле) однородности изучаемого вещества. Интенсивность же каждого из компонентов сложной по своему составу линии испускания пропорциональна числу атомов переходного элемента, участвующих в образовании того или иного окисла. [36]
Поэтому сложная структура основного края поглощения атомов переходных элементов в металлах рассматривалась, так же как и в случае поглощения атомами в молекулах, как результат суперпозиции истинного края поглощения ( в первом приближении описываемого арктангенсоидой) и селективных длинноволновых линий, появление которых обусловлено особым характером заполненияЗй - полосыв металлах этих элементов. К числу экспериментальных фактов, которые можно рассматривать как наиболее веские доказательства справедливости описанного выше взгляда на структуру края поглощения атомов переходных элементов в металлах, относятся результаты сравнительного изучения структуры краев поглощения элементов в различных рентгеновских сериях. В самом деле, допустим, что появление длинноволновой линии в пределах основного К-края поглощения действительно связано с селективным перебросом К-электронов атома на свободные 3 с. Тогда такой переход будет представлять собой квадрупольный, относительно маловероятный переход и может объяснить появление лишь слабой по интенсивности линии поглощения. Если такая линия все-таки наблюдается на опыте, то для этого нужно предположить специальный вид функции, передающей зависимость плотности состояний от энергии. Она должна иметь максимум в области энергий, отвечающих 3 rf - уровням атома в металле. [37]
Интересно, что эту структуру могут образовывать атомы переходных элементов различных групп периодической системы. Обычно эти структуры образуются переходными элементами Mn, Fe, Co, Ni, Pd и Pt, но известны системы с переходными элементами, принадлежащими к группам с меньшим номером. [39]
В случае, когда кристалл построен из атомов переходных элементов, в нем возможно сохранение независящего от / / магнитного момента. При этом различают 4 основных типа кристаллов: J) металлпч. [40]
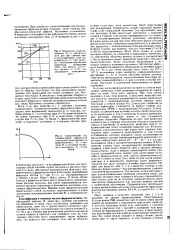 |
Схематический ход температурной зависимости спонтанной намагниченности ферромагнети ка. М - - значение М, в состоянии магнитного насыщения, Тс - точка Кюри. [41] |
В случае, когда ферромагнетик построен из атомов переходных элементов, в нем возможно сохранение не зависящего от внеш. [42]
Экспериментальное изучение магнитных свойств комплексных соединений, включающих атомы переходных элементов, давно уже позволило установить две группы комплексов. В одной из этих групп магнетизм центрального иона оказывается таким же, как и у простых галогевидов, и соответствует наличию от одного до четырех неспаренных электронов на периферийных оболочках атомов в соединении. Комплексные соединения, относящиеся к другой группе, диамагнитны, так что магнитные свойства центрального атома в комплексе резко отличаются от свойств атома в свободном состоянии или в простых солях. Параллельно этому отмечается и различная химическая активность обоих типов комплексов. Принято считать, что в первой группе соединений взаимодействие между центральным атомом и координирующимися вокруг него группами значительно менее глубокое, чем во второй. Если в первой группе соединений взаимодействие сводится в основном к силам ионно-диполыюго притяжения и в меньшей мере связано с вовлечением в кова-лентную связь глубоко лежащих 3 rf - электронов атомов переходных элементов, то устойчивость второй группы соединений, как правило, связана с вовлечением в ковалентную связь всех внешних неспаренных электронов этих атомов, что приводит к коренному изменению структуры электронных оболочек центрального иона. Рассматриваемые комплексы [ Ni ( NH3) 4 ] и [ № ( СМ) 4 ] - - как раз и относятся к обеим указанным группам соединений. Первый из этих комплексов парамагнитен, второй - диамагнитен. Первый представлнет собой, невидимому, тетраэд-рический комплекс, второй, как это установлено, имеет плоскую структуру. [43]
Наконец, следует отметить, что в атомах переходных элементов электроны на различных Sd-орбиталях могут иметь одинаково направленные спины. Так как каждый спин можно уподобить маленькому магнитику, то вследствие сложения нескольких таких спинов атом в целом может приобрести заметные магнитные свойства. [44]
В молекулах типа XYn, где X - атом переходного элемента с внешними d - ( или / -) электронами, а также в комплексах переходных металлов в кристаллах п растворах наблюдаемые энергетические уровни часто определяются лишь только этими d - ( пли / -) электронами. Используя вышеприведенные рассуждения, легко можно получить все состояния, которые соответствуют конфигурациям заданного числа ( / - электронов в поле остова молекулы данной симметрии или в кристаллическом поле, окружающем комплексный ион. [45]
Страницы: 1 2 3 4
