Атом - переходный элемент
Cтраница 2
Для атомов переходных элементов отмечаются две тенденции, определяющие в конечном итоге их химические свойства. С одной стороны, заполняющиеся внутренние / - или / юрбитали по мере увеличения в них числа электронов способствуют экранированию внешних ns - электронов, в силу чего их связь с ядром должна ослабляться. Но, с другой стороны, рост числа электронов на внутренних уровнях приводит к уменьшению атомного радиуса. Наиболее ярко это явление выражено у лантаноидов и получило, как известно, название лантаноидной контракции. В результате контракции связь внешних электронов с ядром должна усиливаться. [16]
В оксиборидах атом переходного элемента должен образовать пять ковалентных и две донорно-акцепторные связи с мостиковыми атомами. Поэтому X может быть элементом V-VIII групп, причем его вторая я-связь с атомами В ( обозначена пунктиром) может иметь различную природу. [17]
В нитридоборидах атом переходного элемента должен образовывать шесть ковалентных и одну донорно-акцептор-ную связь с мостиковыми атомами, так что X может быть элементом VI-VIII групп. Все рассуждения, приведенные для оксиборидов, остаются в силе и для нитридоборидов. [18]
Потенциалы ионизации атомов переходных элементов изменяются с изменением атомного номера гораздо медленее, чем потенциалы ионизации элементов главных подгрупп. Это обусловлено сильным экранированием потенциала ядра, действующего на один из d - электронов, другими d - электронами. [19]
Если агрегация атомов переходных элементов имеется в этих твердых растворах, то по мере снижения концентрации переходного элемента в растворе темп дезагрегации его атомов будет уменьшаться, а за счет этого будет снижаться и скорость роста парамагнитной составляющей восприимчивости. [20]
Однако для атомов переходных элементов эти свойства маскируются более сильными парамагнитными свойствами. Примером чисто диамагнитных веществ могут служить NaCl, H20, С2Н5ОН, инертные газы. [21]
Потенциалы ионизации атомов переходных элементов изменяются с изменением атомного номера гораздо медленее, чем потенциалы ионизации элементов главных подгрупп. Это обусловлено сильным экранированием потенциала ядра, действующего на один из flf - электронов, другими cf - электронами. [22]
 |
Элементарная ячейка структуры типа NiAs. 1-атомы Ni. 2 - атомы As. 3 - сдвоенные тетраэдрические. [23] |
Помимо внедрения атомов переходного элемента в сдвоенные тетраздрические пустоты возможен и другой тип дефектов - вакансии в октаэдрических позициях. [24]
Что касается атомов переходных элементов ( 12), то они также проявляют ряд сходных свойств. Их общей особенностью является слабая зависимость от Z, что связано с тем, что в них заполняется внутренняя подоболочка. Полное объяснение химических свойств этих элементов, а также лантанидов и актинидов требует учета более тонких особенностей взаимодействия электронов в атомах, о которых пойдет речь ниже. [25]
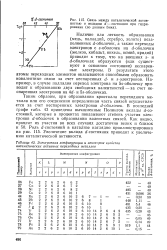 |
Электронная конфигурация и некоторые свойства каталитических активных переходных металлов. [26] |
В результате этого атомы переходных элементов оказываются способными образовать ковалентные связи за счет неспаренных d - и s - электронов. Например, в случае палладия переход электрона на Ss-оболочку приводит к образованию двух свободных валентностей - за счет неспаренных электронов на 4d - и 5з - оболочках. [27]
Наконец, электроны атомов переходных элементов, располагаясь по одному в различных - ячейках, могут иметь одинаково направленные спины и, следовательно, приводить к высоким значениям спинового и магнитного моментов. Таким образом, для переходных элементов должно быть характерно наличие собственных магнитных моментов и, следовательно, высоких значений магнитной восприимчивости. [28]
Наконец, электроны атомов переходных элементов, располагаясь по одному в различных d - ячейках, могут иметь одинаково направленные спины и, следовательно, приводить к высоким значениям спинового и магнитного моментов. Таким образом, для переходных элементов должно быть характерно наличие собственных магнитных моментов и, следовательно, высоких значений магнитной восприимчивости. [29]
Если же электрон теряет атом переходного элемента, то электронная конфигурация возникающего положительного иона отличается от конфигурации любого нейтрального атома. [30]
Страницы: 1 2 3 4