Концевая аминогруппа
Cтраница 3
Наилучший метод установления природы аминокислоты, которой принадлежит концевая аминогруппа пептидной цепи ( N-концевая кислота), состоит в действии на кислоту 2 4-динитрофторбензолом - соединением, высокореакционноспособным при нуклеофильном замещении с участием аминов, но не амидов ( см. гл. В результате этой реакции образуется М-24 - динитрофенильное производное пептида, которое после гидролиза по амидной связи дает N-24 - динитрофениламинокислоту. [31]
Реакция первичных аминов ( нак правило, с концевыми аминогруппами) с азо-тистой кислотой часто приводит к перегруппировкам. Например, при взаимодействии: с азотистой кислотой н-цропиламина образуется смвсь нормального и лзопропидо - вого спиртов. [32]
Метаболит С - А-производное ферриоксамина В, в котором концевая аминогруппа окислена до СООН. [33]
Первый подход, состоящий в постепенном наращивании со стороны концевой аминогруппы ( участок ( а) на схеме, применяется редко, хотя он и имеет прямую аналогию с биосинтезом белка. Он включает удаление защиты карбоксигруппы и активирование концевой карбоксигруппы пептида. Этот подход, следовательно, делает максимальной возможность рацемизации и других возможных побочных реакций, затрагивающих активированный пептид. [34]
Защитные группы для аминной функции используются для М - концевых аминогрупп и для со-аминогрупп лизина и орнитина. Защитные группы этого типа применяются также и для временного блокирования гидразидов ациламинокислот, которые представляют собой промежуточные вещества при получении азидов ( разд. Солеобразование у аминной функции не является действенной защитой в синтезе пептидов. [35]
Низкая молекулярная масса ( 1000 - 3500) и наличие концевых аминогрупп в этих олигоамидах достигается при проведении процесса в избытке амина. [36]
Наличие таких коротких протеиновых цепей и вытекающая из этого доступность концевых аминогрупп обеспечивают способность связывать кислоту, значительно превышающую 80 миллиэквивалентов на 100 г сухой шерсти, определенную по изменению рН раствора при обработке шерсти кислотой и обусловленную наличием основных боковых цепей лизина, аргинина и гистидина. [37]
Количество фиксированного волокном красителя обычно превышает суммарное содержание в нем концевых аминогрупп. [38]
Количество аммиака, получающегося при деструкции полиамидов, также превышает количество концевых аминогрупп в исходном полимере. [39]
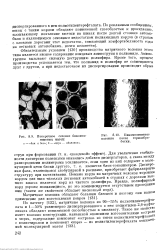 |
Поперечное сечение бикомпо-нентных нитей. [40] |
Обязательным условием [130] производства матричного волокна этого типа является низкое содержание концевых аминогрупп в полиамиде. Аминогруппы вызывают сильную деструкцию полиэфира. [41]
При использовании в качестве аминосодержащих реагентов алифатических аминов или олигомеров с концевыми аминогруппами аналогичным путем получают соответствующие хинонсодержащие полимеры, которые при 120 - 150 С превращаются в сетчатые полимеры. [42]
В качестве отвердителей эпоксидных олигомеров широкое применение нашли низкомолекулярные олигоамиды с концевыми аминогруппами - олигоамидоамины. Их получают поликонденсацией алифатических полиаминов с производными алифатических кислот, например с димеризованными метиловыми эфирами жирных кислот растительных масел. Технология получения таких олигомеров рассмотрена в гл. [43]
Окрашивать пептиды после колонки можно нингидрином, но при этом необходимо освободить концевые аминогруппы пептчдов от возможных модификаций и разрушить пролин, если он окажется на конце пептида. Полагаться при регистрации на УФ-поглоще-ние при 280 нм рискованно, так как в некоторых пептидах может не оказаться остатков ароматических аминокислот. Регистрация при 206 - 220 нм - наиболее надежный метод. [44]
Петере и Спикмэн нашли, что даже суммарное содержание боковых цепей и концевых аминогрупп не может объяснить наблюдаемую способность связывать кислоту. Поэтому они пришли к выводу, из что мембранное равновесие Доннана дает более точное представление о сущности кислотного крашения шерсти, чем теория Джильберта - Райдила. [45]
Страницы: 1 2 3 4