Аномерной атом - углерод
Cтраница 1
Аномерные атомы углерода в а - и J-формах имеют противоположные конфигурации. [1]
Конфигурация аномерного атома углерода приводит к тому, что макромолекула целлюллозы имеет строго линейное строение. Этому способствует образование водородных связей внутри цепи, а также между соседними цепями. [2]
Хиральный центр при аномерном атоме углерода не является единственным в моносахаридах. Для их изображения можно использовать любые из приведенных выше типов формул, но только кон-формационные формулы отображают взаимное пространственное расположение групп, присоединенных к кольцу. [3]
Гидроксильную группу при аномерном атоме углерода в отличие от остальных спиртовых групп называют гликозидной гидроксиль-ной группой. В фишеровских проекциях в D-ряду гликозидный гидро-ксил а-формы располагают справа, а в р-форме - слева. Для Сахаров L-ряда используют обратное правило. [4]
Гликозидная связь осуществляется между аномерным атомом углерода С-1 рибозы ( или дезоксири-бозы) и атомом азота N-1 пиримидинового и N-9; пурино-вого оснований. Природные нуклеозиды всегда являются ( J-ано-мерами. [5]
В результате образуются полуацетали с R - и S-конфи-гурациями аномерного атома углерода. Другими словами, основная причина одновременного образования а - и р-аномеров состоит в нестереоселективности протекающей вне организма реакции. [6]
Образование полуацеталя приводит к появлению нового хирального центра, называемого аномерным атомом углерода или аномсрным центром. [7]
Хотя в свое время ИК-опектроскотшя пираноидных производных облегчила определение конфигурации при аномерном атоме углерода [9, 17], теперь эту проблему гораздо легче решить методом ЯМР-спе Ктро-скопии ( разд. [8]
Исследование ИК-спектров оказывается, таким образом, полезным для определения конфигурации и конформации аномерных атомов углерода; однако в настоящее время для той же цели с большим успехом используется ЯМР-спектроскопия ( разд. [9]
Два циклических полуацеталя о-глюкозы отличаются лишь конфигурацией у углеродного атома в положении 1, аномерного атома углерода, и называются аномерами. Различные изомерные формы D-ГЛЮКОЗЫ более удобно представлять в виде формул Хеуорса ( рис. 11.4 6), хотя даже они дают лишь слабое представление о действительной форме молекул, поскольку шестичленные циклы на самом деле изогнуты ( рис. 11.4 в), как в циклогексане ( гл. [10]
Внутримолекулярное замыкание цикла в циклическую полуаце-тальную структуру связано с возникновением нового хирального центра, аномерного атома углерода. Из одной энантиомерной оксоформы вследствие этого могут образоваться, смотря по обстоятельствам две хиральные диастереомерные циклические полуацетальные формы, которые называют аномерами. [11]
Заметим, что сахароза - это невосстанавливающий сахар, так как два моносахаридных остатка связаны своими аномерными атомами углерода. [12]
Если данный сахар существует в пиранозной форме, то вклад каждого асимметрического углеродного атома, за исключением аномерного атома углерода, в молекулярное вращение должен быть приблизительно одинаковым как в случае а - и р-форм сахара, так и для а - и [ 5-форм метилглюкозида. Следовательно, сумма Л1а Мр для сахара и глюкозида будет одной и той же, если они имеют одинаковую структуру кольца, б) Раскрытие эпоксидного цикла происходит по транс-механизму с обращением конфигурации атома углерода, подвергающегося атаке ( см. I, разд. [13]
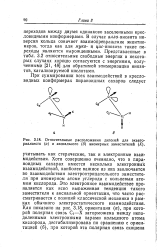 |
Относительные расположения диполей для экваториального ( и и аксиального ( б аномерных заместителей ( А. [14] |
Хотя совершенно очевидно, что в пираноидных сахарах имеется несколько электронных взаимодействий, наиболее важное из них заключается во взаимодействии электроотрицательного заместителя при аномерном атоме углерода с кольцевым атомом кислорода. Это электронное взаимодействие проявляется как ясно выраженная тенденция такого заместителя к аксиальной ориентации, что часто рассматривается с позиций классической механики в рамках обычного электростатического взаимодействия. [15]
Страницы: 1 2 3