Кратность - связь
Cтраница 1
 |
Виды атомов без полного учета окружения. [1] |
Кратность связи - характеристика, возникшая в классической теории химического строения. В квантовой химии это понятие вводится пока с большими натяжками. [2]
Кратность связи зависит от ее длины и электронной плотности. [3]
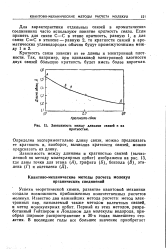 |
Зависимость между длинами связей и их кратностью. [4] |
Кратность связи зависит от ее длины и электронной плотности. Так, например, при одинаковой электронной плотности двух связей большую кратность будет иметь более короткая. [5]
Кратность связи обусловлена наложением на ст-связь л - и 6-связей. [6]
Кратность связи в молекуле СО также равна трем. Разрыхляющее действие МО подавлено. Молекула СО также относится к числу прочных. Межъядерное расстояние невелико, а энергия диссоциации высока. [7]
Кратность связи определяется количеством электронных пар, связывающих два атома. Так, в этане Н3С - СН3 связь между атомами углерода одинарная, з этилене Н2С СН2 - двойная, в ацетилене НС СН - тройная. С увеличением кратности связи увеличивается энергия связи: энергия связи С - С составляет 263 3 кДж / моль, С С - 422 2 кДж / моль и С С - 535 кДж / моль. [8]
Кратность связи определяется количеством электронных пар, связывающих два атома. Так, в этане Н3С - СН3 связь между атомами углерода одинарная, в этилене Н2С СН2 - двойная, в ацетилене НС СН - тройная. С увеличением кратности связи увеличивается энергия связи: энергия связи С-С составляет 263 3 кДж / моль, С С - 422 2 кДж / моль и СС - 535 кДж / моль. [9]
Кратность связи определяется количеством электронных пар, связывающих два атома. Так, в этане Н3С - СН3 связь между атомами углерода одинарная, в этилене Н2ССН2 - двойная, в ацетилене НС СН - тройная. С увеличением кратности связи увеличивается энергия связи: энергия связи С-С составляет 263 3 кДж / моль, СС - 422 2 кДж / моль и С С - 535 кДж / моль. [10]
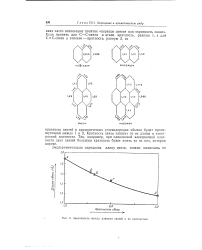 |
Зависимость между длинами связей и их кратностью. [11] |
Кратность связи зависит от ее длины и электронной плотности. [12]
Кратность связи определяется числом электронных пар, связывающих два атома. Например, в этане Н3С - СН3 связь между атомами углерода одинарная, в этилене Н2ССНг - двойная, в ацетилене НС СН - тройная. С увеличением кратности связи энергия связи возрастает. Так, энергия связи С-С, СС и С С составляет соответственно 263, 422 и 535 кДж / моль. [13]
Кратность связи равна единице. [14]
Кратность связи М - N в комплексах второй группы, в целом, выше, чем в комплексах первой группы; соответственно и расстояние М - N оказывается короче на - 0 25 А. [15]
Страницы: 1 2 3 4