Разделенный атом
Cтраница 1
СН из разделенных атомов углерода и водорода; hh - теплота расщепления молекулы водорода); i, vt, vs - теплоты образования из атомов соответственно одинарной, двойной и тройной связей СС; ж, у, z - число этих связей в мояекуле углеводорода. [1]
 |
Предсказанные основное и возбужденные состояния С2. [2] |
При переходе от разделенных атомов к молекуле должны соблюдаться некоторые общие правила корреляции в отношении типов электронных состояний, впервые развитые Вигнером и Витмером. [3]
 |
Корреляционная диаграмма для двух одинаковых атомов. [4] |
Расположение энергетических уровней разделенных атомов, объединенного атома и того промежуточного образования, которое является молекулой, различно. [5]
Из W одинаковых уровней у далеко разделенных атомов в твердом тело образуется энергетическая зона, состоящая из близко расположенных N различных уровней. Напомним, что в 1 см твердых тел содержится примерно 1022 - 1023 атомов. Все огромное количество электронов того куска твердого тела, с которым мы экспериментируем, коллективизируется и представляет собой единую систему, подчиняющуюся тем же общим квантовым законам, что и немногочисленная система электронов отдельного атома. Но вместо узкого уровня отдельного атома, вмещающего не более двух электронов ( если уровень не вырожден), в твердом теле образуются широкие энергетические полосы, число уровней в которых равно числу атомов в куске твердого тела. [6]
Эти два предельных случая называются соответственно разделенными атомами и объединенным атомом. При медленном изменении расстояния между протонами от R со до R 0 состояния разделенных атомов должны непрерывно переходить в состояния объединенного атома в соответствии с адиабатическим принципом. [7]
Соотношение между молекулярными состояниями и состояниями разделенных атомов более сложное. [8]
В результате из N одинаковых уровней у далеко разделенных атомов в твердом теле возникает энергетическая зона, состоящая из N близко расположенных, но тем не менее различных уровней. Образование энергетических зон при сближении атомов показано на рис. 1.1 для натрия. Здесь по оси абсцисс отложено расстояние между соседними атомами; га - соответствующее равновесное расстояние в твердом теле. [9]
Если энергия молекулярной орбиты ниже энергии соответствующего уровня разделенных атомов, то такая молекулярная орбита называется связывающей. Если энергия молекулярной орбиты равна энергии соответствующего уровня разделенных атомов, то такая молекулярная орбита называется несвязывающей. И, наконец, молекулярная орбита называется разрыхляющей, если ее энергия лежит выше энергии соответствующего уровня разделенных атомов; разрыхляющие орбиты обозначаются знаком, стоящим справа сверху у символа орбиты. [10]
Ниже все молекулярные орбитали классифицированы на основе терминологии разделенных атомов, хотя для Не. [11]
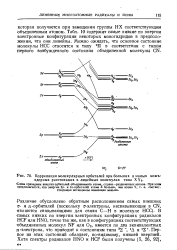 |
Корреляция молекулярных орбнталей при больших и малых межъядерных расстояниях в линейных молекулах типа XYa. [12] |
Огева приведены энергии орбиталей объединенного атома, справа - разделенных атомов. [13]
Последняя есть сумма плотностей зарядов двух пар электронов в разделенных атомах. [14]
Волновая функция МО определяется по методу ЛКАО с использованием АО разделенных атомов. После значения А ( а л; или б) указывают главное и азимутальное квантовые числа для разделенных атомов. [15]
Страницы: 1 2 3 4