Диаграмма - потенциальная энергия
Cтраница 3
На рис. 3 - 1, а изображена диаграмма потенциальной энергии электронов, соответствующей уровню Ферми для данного металла. Работа выхода из металла определяется как работа, необходимая для переноса электрона с уровня Ферми в вакуум на достаточно удаленное расстояние от поверхности. [31]
Хотя мы ограничили наше рассмотрение только двумя нормальными колебаниями, диаграмма потенциальной энергии, имеющая много измерений, очевидно, может быть разложена на подобные трехмерные диаграммы. [32]
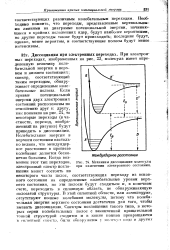 |
Механизм диссоциации молекулы при изменении электронного состояния. [33] |
Необходимо помнить, что переходы, представленные вертикальными линиями на диаграмме потенциальной энергии, начинающиеся в крайних положениях ядер, будут наиболее вероятными, но другие переходы также будут происходить; последние будут, однако, менее вероятны, и соответствующие полосы будут менее интенсивны. [34]
Взаимодействие молекулы типа На с поверхностью металла можно проиллюстрировать при помощи диаграммы потенциальной энергии /, представленной на рис. 1, где кривые / и 2 выражают потенциальную энергию молекулы в зависимости от ее удаленности от поверхности металла. Поведение молекулы, приближающейся к поверхности, зависит от относительного положения обеих кривых. Если, однако, молекула может приобрести энергию активации, равную или превосходящую Еа, то тогда в точке S возможен переход на кривую 2 и молекула будет адсорбирована в атомарном состоянии. [35]
На рис. 4.5 показано, как такие сольвата-ционные эффекты могут изменить диаграмму потенциальной энергии и вызывать изменения скорости при переходе от растворителя к растворителю, К сожалению, в настоящее время яе существует какой-либо общей теории для корреляции или предсказания таких специфических сольватационных эффектов. [36]
Квантовомеханическое рассмотрение подтверждает принцип Франка - Кондона: вертикальные переходы на диаграмме потенциальной энергии действительно оказываются наиболее вероятными. Напомним, что осциллятор, соответствующий реальной молекуле, никогда не бывает в состоянии покоя, а вероятность распределения колеблющихся масс на нулевом колебательном уровне ( v 0) определяет область возможных расстояний между ядрами в этом состоянии. [37]
Каждая из 3N - 6 нормальных координат может быть представлена своей собственной диаграммой потенциальной энергии, подобно показанной на рис. 5.3. В этом случае абсциссой является нормальная координата, а не межатомное расстояние. [38]
Эта модель легко может быть описана с помощью приведенной на рис. 1 диаграммы потенциальной энергии. Эта диаграмма иллюстрирует зависимость потенциальной энергии системы, состоящей из радикала R - и молекулы А, от расстояния между R - и А. [39]
Связь между теорией переходного состояния и механизмом реакции часто иллюстрируют с помощью диаграмм потенциальной энергии. Диаграммы потенциальной энергии для гипотетических одностадийной бимолекулярной и двустадийной реакций показаны на рис. 4.1. Нижняя диаграмма изображает двустадийную реакцию, в которой участвует интермедиат, обладающий конечным временем жизни. В таком случае имеется два переходных состояния. Более высокая энергия активации первого переходного состояния на нижней диаграмме подразумевает. [40]
Соотношения, связанные с величиной энергии активации, удобно рассматривать с помощью диаграмм потенциальной энергии. На рис. 1.6 схематически изображено сечение поверхности потенциальной энергии вдоль пути реакции. Кривая 2 соответствует более высокому потенциалу, чем кривая 1, и соответственно меньшей энергии активации. [41]
АВ представляет собой активированный комплекс, имеющий конфигурацию, соответствующую седловине на диаграмме потенциальной энергии, a v - скорость его распада. [42]
X проходит через перевальную точку ( седловину, точку минимакса) на диаграмме потенциальной энергии; хх - трансмиссионный коэффициент, или вероятность того, что X, достигший перевальной точки, не распадается снова на реагирующие вещества; / х, / А) - коэффициенты активности соответствующих частиц. [43]
АВ представляет собой активированный комплекс, имеющий конфигурацию, соответствующую седловине на диаграмме потенциальной энергии, a v - скорость его распада. [44]
X проходит через перевальную точку ( седловину, точку минимакса) на диаграмме потенциальной энергии; хх - трансмиссионный коэффициент, или вероятность того, что X, достигший перевальной точки, не распадается снова на реагирующие вещества; / х, / А - коэффициенты активности соответствующих частиц. [45]
Страницы: 1 2 3 4 5