Диаграмма - потенциальная энергия
Cтраница 4
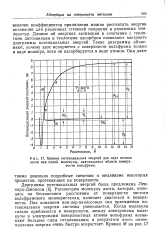 |
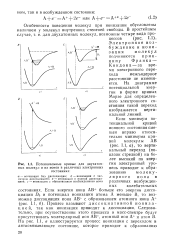
Кривые потенциальных энергий для двух атомов азота или одной молекулы, находящихся вблизи поверхности вольфрама. [46] |
Данные об энергиях активации в сочетании с тепло-тами диссоциации и теплотами адсорбции позволяют построить диаграммы потенциальных энергий. Такие диаграммы объясняют, почему азот испаряется с поверхности вольфрама только в виде молекул, хотя он адсорбируется в виде атомов. [47]
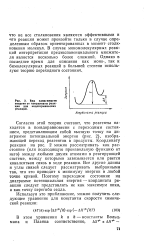 |
Вид зависимости энергии от координаты реакции для эндотермических реакций. [48] |
Согласно этой теории считают, что реагенты находятся в псевдоравновесии с переходным состоянием, представляющим собой высшую точку на диаграмме потенциальной энергии ( рис. 2), изображающей переход реагентов в продукты. Координату реакции на рис. 2 можно рассматривать как расстояние ( или подходящую произвольную функцию от него) между любыми двумя атомами в реагирующей системе, между которыми завязывается или рвется ковалентная связь в ходе реакции. Все другие длины и углы связей следует рассматривать выбранными так, что это приводит к минимуму энергии в любой точке кривой. Поэтому переходное состояние на диаграмме потенциальная энергия - координата реакции следует представлять не как максимум пика, а как точку перегиба седла. [49]
Возможность того, что такое сочетание энергий может играть большую роль в проблеме кинетики реакций, признавалась еще раньше, чем была найдена возможность изображать эту зависимость в виде диаграмм потенциальной энергии. [50]
Связь между теорией переходного состояния и механизмом реакции часто иллюстрируют с помощью диаграмм потенциальной энергии. Диаграммы потенциальной энергии для гипотетических одностадийной бимолекулярной и двустадийной реакций показаны на рис. 4.1. Нижняя диаграмма изображает двустадийную реакцию, в которой участвует интермедиат, обладающий конечным временем жизни. В таком случае имеется два переходных состояния. Более высокая энергия активации первого переходного состояния на нижней диаграмме подразумевает. [51]
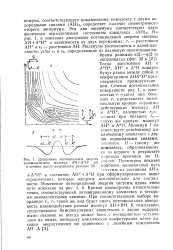 |
Диаграмма потенциальной энергии. [52] |
АН) 2, определяет наличие симметричного второго минумума. На рис. 1, а показана диаграмма потенциальной энергии системы АН А Н в зависимости от двух переменных: г - расстояния АН и г2 - расстояния АН. [53]
При этом А является любой формой активных частиц, которые могут возникнуть при активации молекул А; при дезактивации возбужденных частиц А могут образоваться только молекулы А. Эту схему можно представить в виде диаграммы потенциальной энергии, как показано на рис. XI.1, где приведено сечение поверхности потенциальной энергии, соответствующее минимальным величинам U для различных величин L. Как следует из рис. XI.1, реакция эндотермична, так как минимум энергии для В располагается выше, чем минимум энергии для А. Разность этих двух энергий соответствует тепловому эффекту реакции А. [54]
Если существует некий путь между реагентами и продуктами, которому отвечает более низкий максимум энергии, чей любым другим, то именно по этому пути и пойдет реакция. Именно этот путь и наносят на диаграмму потенциальной энергии. Кривая на графике потенциальной энергии представляет собой этот путь с наименьшей энергией, проходящий через поверхность, которая может быть построена путем рассмотрения зависимости энергии от изменения пространственного расположения атомов, участвующих в реакции. Из теории переходного состояния естественно вытекает принцип микроскопической обратимости, согласно которому тот же самый путь, который реакция проходит в прямом направлении, может быть пройден и в обратном направлении, так как он отвечает самым низкам барьерам энергии для обоих процессов. Следовательно, информация о природе переходного состояния или интермедиата, полученная при исследовании прямой реакции, применима и к обсуждению обратного процесса, происходящего в тех же условиях. [55]
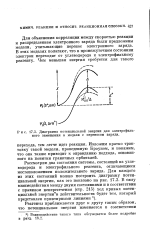 |
Диаграмма потенциальной энергии для электрофиль-ного замещения в модели с переносом заряда. [56] |
Рассмотрим два состояния системы, состоящей из углеводорода и электрофильного реагента, отличающиеся местоположением положительного заряда. Для каждого из этих состояний можно построить диаграмму потенциальной энергии, как это показано на рис. 17.3. В силу взаимодействия между двумя состояниями и в соответствии с правилом непересечения ( стр. [57]
В этой главе ставилась задача показать, какой свет могут пролить методы теории валентности на скорости реакций. Отмечалось, что эти методы не могут применяться для вычисления абсолютных скоростей реакций, в лучшем случае они могут только дать информацию о диаграммах потенциальной энергии. Тем не менее, как видно теперь, хотя и нельзя сделать точных предсказаний, приближенные методы, подобные методу Хюккеля, создают весьма полезную основу для обсуждения экспериментальных результатов. [58]
Прежде всего это адсорбция, которая обсуждается в гл. В этой главе мы рассмотрим различные типы изотерм адсорбции в связи с зависимостью величины теплоты адсорбции от степени заполнения поверхности; обсудим вопрос об энергетике адсорбции на основании анализа диаграмм потенциальной энергии. [59]
 |
Потенциальные кривые для двухатомных молекул и их ионов в различных электронных состояниях. [60] |
Страницы: 1 2 3 4 5