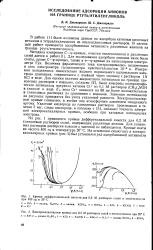
Кривая - дифференциальная емкость
Cтраница 3
Минимум на кривых дифференциальной емкости хорошо совпадает с максимумом электрокапиллярных кривых. [31]
В первом приближении кривые дифференциальной емкости на твердых электродах в присутствии органических соединений аналогичны соответствующим кривым на жидкой ртути. При адсорбции органических молекул, которая имеет место при не слишком больших зарядах поверхности, наблюдается снижение емкости по сравнению с емкостью в чистом растворе фона, а при увеличении заряда электрода имеет место десорбция органического вещества, сопровождающаяся характерным пиком на кривых дифференциальной емкости. Пики на С, - кривых в случае твердых электродов выражены хуже, чем в случае жидкой ртути ( см. рис. 30), что, возможно, связано с неоднородностью твердой поверхности. [32]
Нами были измерены кривые дифференциальной емкости в следующих растворах к - С4Н9ОН: 0 02; 0 05; 0 07; 0 1; 0 12; 0 15; 0 17; 0 20; 0 25; 0 30; 0 35; 0 4; 0 5; 0 6; 0 7 и 0 8 М на фоне 0 1 N Na2S04 при 25 С. [33]
Нами были измерены кривые дифференциальной емкости ( рис. 6) и зависимости периода капания т от потенциала ср ( рис. 7) в присутствии отдельно ТБА и ГС, а также в присутствии смеси ТБА и ГС. Как следует из рис. 7, величина т, пропорциональная пограничному натяжению, снижается как в присутствии ТБА ( кривая 3), так и в присутствии ГС ( кривая), причем ТБА адсорбируется преимущественно в области отрицательных зарядов-поверхности, а ГС - в области положительных зарядов. Кривая т - ср, измеренная в смеси ГС и ТБА ( кривая 4, рис. 7), лежит ниже кривых 2 и 3, что указывает на совместную адсорбцию ГС и ТБА при небольших зарядах поверхности. [34]
Описанные в литературе кривые дифференциальной емкости ( С - ср-кривые) и электрокапиллярные кривые ( о-ф-кривые) для этих растворителей [4-9 ] относятся к растворам электролитов сравнительно низкой концентрации, не превышающей, как правило, 0 5 N. В данной работе основные измерения были выполнены в растворах LiNO3 от 0 1 N до насыщенного. [35]
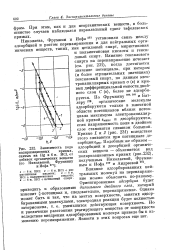 |
Зависимость хода поляризационных кривых, снятых на Hg в 6 н. НС1, от добавок органических веществ ( по Николаевой, Фрумкину и Иофа277. [36] |
&) и кривых дифференциальной емкости двойного слоя С ( е), более не адсорбируется. По Фрумкину 2в4 265 и Бат-леру 278, органические молекулы адсорбируются только в известной области потенциалов вблизи потенциала максимума электрокапиллярной кривой 8Макс и десорбируются, если напряженность поля в двойном слое становится слишком большой. [37]
Для объяснения свойств кривых дифференциальной емкости границы раздела ртуть - водный раствор было введено представление [9] о слое молекул воды с низким значением эффективной диэлектрической проницаемости и толщиной, соизмеримой с молекулярными размерами - слое, находящемся между поверхностью металлической фазы и объемом водного раствора. [38]
Наконец, измерениями кривых дифференциальной емкости ртутного капельного электрода в контакте с концентрированным раствором сульфида [16] адсорбция сульфид-ионов на ртути не обнаружена. [39]
На рис. 24 представлены кривые дифференциальной емкости на базисной плоскости скола пирографита. С, - Кривая имеет параболическую форму и почти симметрична по отношению к точке минимума. При этом в концентрированных растворах дисперсия емкости от частоты переменного тока практически отсутствует. Близкая величина емкости в минимуме - 4 мк Ф / см2 была получена в работе [174] при исследовании электрокапиллярных свойств этого же монокристаллического пирографита путем измерения высоты мениска. [40]
На рис. 1 приводятся кривые дифференциальной емкости для 0 2 М гликолевых растворов солей, содержащих различные анионы. Для указанных растворов дисперсия емкости с частотой не наблюдается. Кривые сняты на частоте 400 щ и температуре 20 С. [42]
При 20 С измерены кривые дифференциальной емкости, электрокапиллярные кривые, величины поверхностного натяжения на границе раствор / воздух, а также эквивалентные электропроводности и вязкости для растворов LiNO3 н формамиде, N-метилформамиде и диметилформамиде в интервале концентраций от О, N до насыщенного. На основе полученных данных установлено, что строение двойного электрического слоя на границе между ртутью и концентрированными растворами LiNO3 в этих растворителях может быть интерпретировано в рамках предположения о сильной сольватации ионов Ц и NO при наличии сил зеркального изображения, уменьшающих толщину диэлектрической прослойки между поверхностью электрода и ионной обкладкой двойного слоя. [43]
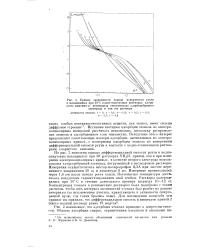 |
Кривые зависимости заряда поверхности ртути в насыщенных при 30 С водно-этаноловых растворах хлористого аммония от потенциала относительно хлорсеребряного электрода в том же растворе. [44] |
На рис. 2 показаны кривые дифференциальной емкости ртути в водно-спиртовых насыщенных при 30 растворах NH4G1, причем, как и при измерении электрокапиллярных кривых, в качестве второго электрода использовался хлорсеребряный электрод, погруженный в исследуемые растворы. [45]
Страницы: 1 2 3 4 5