Частная поляризационная кривая
Cтраница 2
Настоящая работа посвящена изучению совместного разряда цинка и кобальта из сернокислых электролитов методом построения частных поляризационных кривых. [16]
Таким образом, возможность пассивации цементирующего металла в ходе процесса определяется не только взаимным расположением и параметрами частных поляризационных кривых, о и характерам образующегося осадка. [17]
Фактически общая поляризационная кривая должна пройти выше, чем если бы она была получена путем аддитивного суммирования ординат частных поляризационных кривых. [18]
Эти уравнения описывают зависимость скорости либо толью катодного, либо только анодного процесса от потенциала и на зываются уравнениями частных поляризационных кривых. [19]
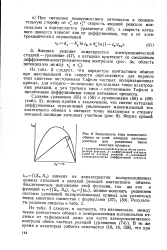 |
Зависимость тока контактного. [20] |
Из табл. 2 следует, что параметры контактного обмена при максимальной его скорости определяются для первого типа кинетики постоянными Тафеля частных поляризационных кривых, для второго-величинами предельных токов электродных реакций, а для третьего типа - постоянными Тафеля и предельным диффузионным током катодного процесса. [21]
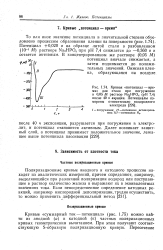 |
Кривая потенциал - - время для стали при погружении в 0 05 М раствор Na2HPO4 ( рН 7 4 после 40 ч аэрации. Потенциалы измерены относительно водородного электрода. [22] |
Кривые суммарный ток - потенциал ( рис. 1.75) можно найти из анодной ( а) и катодной ( к) частных поляризационных кривых геометрическим вычитанием. При этом получают соответствующую S-образную поляризационную кривую. [23]
Соотношение между током, идущим на разряд хлора, и током, идущим на выделение кислорода, оп - ределяется характером частных поляризационных кривых. [24]
 |
Кривая потенциал - - время для стали при погружении в 0 05 М раствор Na2HPO4 ( рН 7 4 после 40 ч аэрации. Потенциалы измерены относительно водородного электрода. [25] |
Кривые суммарный ток - потенциал ( рис. 1.75) можно найти из анодной ( а) и катодной ( к) частных поляризационных кривых геометрическим вычитанием. При этом получают соответствующую S-образную поляризационную кривую. [26]
Чтобы располагать полной картиной возможности совместного разряда ионов различных примесей с ионами очищаемого металла, необходимо исследовать условия перехода в катод каждой отдельной примеси в паре с очищаемым металлом и на основании полученных частных поляризационных кривых, совместного разряда иметь суждение о характере процесса совместного разряда ионов всех примесей вместе с очищаемым металлом ( см. примеры, приведенные в гл. [27]
Таким образом, в случае замедленной электрохимической стадии цементации для каждой пары металлов существует вполне определенный максимальный ток контактного обмена, наблюдаемый в момент, когда отношение площадей катодных и анодных участков поверхности становится равным отношению наклонов частных поляризационных кривых. Формулы для вычисления этих параметров, представленные в табл. 2, выведены для следующих трех различных типов кинетики цементации. [28]
Сопоставление частных поляризационных кривых с зависимостью компромиссного потенциала от времени для различных концентраций CuSO4 - 5H2O ( рис. 4 5) показало, что при содержании соли до 20 г / л процесс проходит с катодным диффузионным контролем. Скорость осаждения меди постоянна во времени и равна предельной диффузионной плотности тока. [29]
Температурно-кинетический метод, как и метод вращающегося диска, не дает ответа на вопрос о том, какой из частных процессов ( анодный или катодный) в большей степенл контролирует скорость цементации; и какая именно. Электрохимический метод основан на сопоставлении частных поляризационных кривых катодного и анодного процессов с областью потенциалов, в которой проходит контактный обмен. [30]
Страницы: 1 2 3