Кольцевой атом - азот
Cтраница 3
Все шестичленные полностью ненасыщенные гетероциклические соединения можно представить как бензол, у которого один или более атомов углерода заменены на гетероатом. Пиридин ( азабен-зол) - простейший из подобных соединений - имеет один кольцевой атом азота. Подобно бензолу, молекула пиридина представляет собой плоскую циклическую систему, слегка искаженный шестиугольник из-за меньшей длины связи С-N по сравнению со связями С-С. Ее можно представить ( рис. 2.1, а) как циклическую систему, состоящую из пяти р2 - гибридизованных атомов углерода, к каждому из которых присоединен атом водорода ( на рисунке не показаны), и одного 5р2 - гибридизованного атома азота. Каждый из шести атомов кольца имеет одну р-орбиталь, перпендикулярную плоскости кольца. Эта структура подобна структуре бензола по наличию единого цикла р-орбиталей, содержащего шесть электронов, но отличается тем, что обладает неподеленной парой электронов в плоскости кольца. Подобно бензолу, молекулу пиридина удобно представить в виде одной из двух эквивалентных структур Кекуле. [31]
Образование 4 - ( п-нитробензил) изохинолина ( X) при нитровании 4-бензил-изохинолина ( IX) [314] указывает на то, что изохинолиновое ядро менее реак-ционноспособно при нитровании, чем замещающая бензильная группа. Однако дезактивирующее действие нитрогруппы на бензольное кольцо оказывается сильнее, чем дезактивирующее действие кольцевого атома азота в гетероциклическом ядре изохинолина, и поэтому следующая нитрогруппа вступает в положение 5 ( или 8) изохинолинового ядра, а не в иитробензильный остаток. [32]
В гетероароматических соединениях встречаются некоторые другие типы прототропной таутомерии, примеры приведены на рис. 2.21. Для 3-гидроксипиридина в растворе устанавливается равновесие с оксидом пиридиния ( рис. 2.21, а), так как не существует нейтрального таутомера пиридона. Внутримолекулярные тауто-мерные переходы в полностью ароматических структурах, связанные с протонированием и депротонированием различных кольцевых атомов азота, как, например, в молекуле 1 2 4-триазола ( рис. 2.21, б), обычно представляют собой быстрые низкоэнергетические процессы. [33]
Можно предположить, что в катионе пири-диниевой соли положительный заряд одновременно находится на кольцевом атоме азота и на а - и у-углеродных атомах кольца. [34]
Можно предположить, что в бромцианиде у-бензоксипири-дина электроны заметно смещены не только в сторону кольцевого атома азота, но и в направлении карбонильного кислорода ( схема на стр. [35]
Сравнение значений рКл, измеренных в тетрагидрофуране [169], демонстрирует, что у-изомеры обладают в большей степени кислотными свойствами, чем а-алкилпиридины, а а - и у-изомеры более сильные кислоты, чем р-изоме-ры, однако образование того или иного аниона при возможности нескольких конкурирующих процессов депротонирования существенно зависит от ряда условий. Гораздо большая склонность [171] сс-и у-алкил-пиридинов кдепротонированию связана с мезомерной стабилизацией соответствующих анионов с участием кольцевого атома азота, что невозможно; р-изомера. В последнем случае депротонированию способствует. [36]
Для аминодиазинов характерно существование в амино-форме. Аминодиазины - более сильные основания, чем соответствующие незамещенные диазины и прото-нируются по одному из двух кольцевых атомов азота, что приводит к образованию двух изомерных катионов. [37]
Пиколины являются до некоторой степени более сильными основаниями, чем пиридин. Это связано в первую очередь с индукционным эффектом метильнои группы, нагнетающей электроны в направлении к кольцевому атому азота. Степень легкости, с которой электронная пара азота захватывает ион водорода, показывает, что основность р - и у-пиколина приблизительно одинакова, тогда как а-пиколин обладает значительно более ярко выраженным основным характером в связи с тем, что здесь метильная группа расположена ближе к атому азота. [38]
В реакциях электрофильного замещения ( сульфирование, нитрование, галоидирование) пиридин ведет себя также несколько иначе, чем незамещенный бензол. Эти реакции протекают значительно труднее, чем в случае бензола, прн-чем заместители вступают в р-положение к кольцевому атому азота. Иначе говоря, пиридин напоминает в этом отношении нитробензол. Например, с КОН пиридин дает калиевую соль i-окси-пиридина. Интересно отметить, что пиридином, как и с нитробензолом, не удается осуществить реакцию Фпиделя - Крафтса. [39]
В реакциях электрофильного замещения ( сульфирование, нитрование, галоидирование) пиридин ведет себя также несколько иначе, чем незамещенный бензол. Эти реакции протекают значительно труднее, чем в случае бензола, причем заместители вступают в - положение к кольцевому атому азота. Иначе говоря, пиридин напоминает в этом отношении нитробензол. При реакциях с нуклеофиль-ными реагентами ( едкое кали, амид натрия), наоборот, замещаются атомы водорода у а - и f - углеродных атомов. Например, с КОН пиридин дает калиевую соль я-окги-пиридина, подобно тому как нитробензол с порошкообразным едким кали дает о-нитрофенол. Интересно отметить, что с пиридином, как и с нитробензолом, не удается осуществить реакцию Фриделя-Крафтса. [40]
 |
Прототропиая таутомерия 2 - и 4-замещеииых пиридииов ( X NR, О или. [41] |
Многие гетероароматические соединения могут существовать в двух или более таутомерных формах. Если в качестве альтернативных мест протонирования выступают два гетероатома, в растворе обычно устанавливается равновесие, обусловленное быстрым внутримолекулярным переносом протона между кольцевым атомом азота и атомом азота, кислорода или серы заместителя, как показано на рис. 2.20 для 2 - и 4-замещенных пиридинов. [42]
Указанные свойства качественно очень близки соответствующим свойствам сериновых протеиназ, и механизмы катализа этими ферментами также очень близки. Данные рентгеноструктур-ного анализа показывают, что HS-группа в активном центре па-паина контактирует с имидазольной группой остатка гистидин а на противоположной стороне впадины ( гистйдин-159), связанного водородной связью через удаленный кольцевой атом азота с амидной группой аспарагина-175. [43]
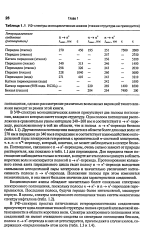 |
УФ-спектры моноциклических азинов ( тонкая структура не приводится. [44] |
Поглощение, связанное с п - я - переходом, очень сильно зависит от природы растворителя, как показано в табл. 1.1 для пиримидина. Для пиридина такое поглощение наблюдается только в гексане, в спирте же эта полоса сдвинута в область коротких волн и маскируется полосой п - я - перехода. Протонирование кольцевого атома азота пиридинового цикла гасит полосу п - я - перехода вследствие связывания неподеленной пары электронов и значительно увеличивает интенсивность полосы п - я - перехода. Положение полосы при этом изменяется э, и она имеет большое значение для характеристики соединений. [45]
Страницы: 1 2 3