Первый атом - хлор
Cтраница 2
Вероятно, в этой реакции вместо бромистого метилена мож но использовать хлористый метилен, поскольку после замещения первого атома хлора второй атом должен замещаться чрезвычайно быстро. Циклизация с образованием пятичленного кольца является благоприятным процессом, а алкилирующим агентом на этой стадии будет алкоксиметилгалогенид. [16]
Атомы хлора в молекулах хлористого цианура подвижны и легко взаимодействуют со спиртами, аминами и фенолами, но подвижность их неодинакова. Первый атом хлора легко подвергается алкоголизу и аммонолизу уже при О С, второй и третий - при более высоких температурах. [17]
Реакции PSC13 со спиртами и фенолами применяют исключительно для синтеза пестицидов. Первый атом хлора замещается при действии спиртов при 20 - 30 С, для замещения второго атома требуется спиртовой раствор щелочи, для третьего - взаимодействие с алкоголятом или фенолятом. [18]
Это соединение является хлорангидридом трехосновной циа-нуровой кислоты, причем подвижность атомов хлора в нем различна. Первый атом хлора замещается при 0 - 5 С, второй - при 20 - 40 С, третий - при 70 - 100 С. [19]
Реакции PSC13 со спиртами и фенолами применяют исключительно для синтеза пестицидов. Первый атом хлора замещается при действии спиртов при 20 - 30 С, для замещения второго атома требуется спиртовой раствор щелочи, для третьего - взаимодействие с алкоголятом или фенолятом. [20]
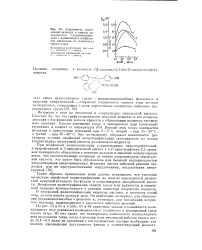 |
Зависимость приведенной вязкости и выхода полиарилатов 1 6-диоксинафта-липа с адишшовой и изофтале-вой кислотами от количества едкого натра. [21] |
Интересен в этом же отношении и хлорапгидрид циануровой кислоты. Первый атом хлора замещается фенолами в присутствии оснований при 0 - 5 С, второй - при 15 - 20 С, а третий - при 30 - 40 С. Это, по-видимому, открывает возможность ( регулируя условия межфазной полиэтерификации) синтезировать на основе хлорапгидрида циануровой кислоты различные полиарилаты. [22]
Сложные эфиры угольной кислоты получают из фосгена. Как и при синтезе фосфатов и тиофосфатов, первый атом хлора в фосгене замещается значительно легче второго. [23]
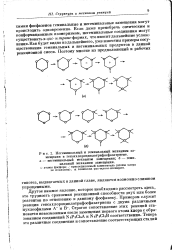 |
Негеминальный и гемивальный механизм замещения в гексахлороциклотрифосфазатриене. а - негеминальный механизм замещения. б - геми-нальный механизм замещения. [24] |
Другое важное явление, которое необходимо рассмотреть здесь, это трудность сравнения реакционной способности двух или более реагентов по отношению к данному фосфазену. Строгое сопоставление этих реакций становится невозможным после замещения первого атома хлора с образованием соединений КзРзСЬА и NsPsCbB соответственно. [25]
Поэтому п-ксилиленхлоргидрин гидролизуется быстрее исходного п-ксилилендихлорида. Таким образом, стадией, лимитирующей скорость реакции, является первая, более медленная стадия замещения первого атома хлора. [26]
На основе температурной зависимости скоростей реакций ДХДФС и 4 - ( 4 метилфенокси -) - 4 -хлордифенилсульфона с 4-крезолятом натрия1 по значениям экспериментальных констант скоростей реакций графическим решением уравнения Аррениуса определены энергии активации реакций, которые составили 80 8 и 108 3 кДж / моль, соответственно. Из полученных данных следует, что в исследуемом диапазоне температур происходит последовательное замещение атомов хлора в ДХДФС на 4-мстилфенокси-группу, при этом первый атом хлора замещается быстрее, чем второй. Соотношение констант скоростей конкурирующих реакций kijk - 2 увеличивается с понижением температуры, которое, таким образом, способствует селективному замещению одного атома хлора. [27]
Однако при замещении одного атома хлора какой-либо группой, например амино -, гидрожси - или хромогеном, активность других атомов хлора снижается. Так, если первый атом хлора реагирует с И-кислотой ( 2-амгано - 5 - гидр01К1СинафтаЛ И Н-7 -: Сульфо1кислота) при 0 - 20 С, то-второй - уже при 40 - 50 С, а третий - только при 90 - 100 С. [28]
Монохлортриазиновый краситель Активный голубой 48 получают взаимодействием бромаминовой кислоты с 4-нитроанилин - 2-сульфокисло-той, восстановлением нитрогруппы в продукте реакции сернистым натрием, ацилированием полученной 1-амино - 4 - ( 4 -амино - 2 -сульфофенил-амино) - антрахинон-2 - сульфокислоты цианурхлоридом ( N3C3C13) в условиях, близких к описанным выше, и замещением второго атома хлора в триазиновом кольце остатком метаниловой или сульфаниловой кислоты. С этой целью в реакционную массу после взаимодействия с цианурхлоридом приливают водный раствор сульфаниловой ( или метаниловой) кислоты и нагревают до 40 С, одновременно добавляя раствор соды для поддержания постоянного рН среды. Эта стадия протекает значительно медленнее замещения первого атома хлора. [29]
Прежде чем сравнивать реакционную способность этих нуклеофильных частиц по отношению к хлорофосфазенам, следует учесть ряд других факторов. Первый из них заключается в том, что необходимо заместить до шести или восьми атомов хлора ну-клеофильными частицами, и эти новые заместители в общем случае последовательно дезактивируют данный фосфазен по отношению к дальнейшему нуклеофильному воздействию. Сила этой дезактивации зависит, конечно, от природы заместителя, и поэхому сравнение различных реагентов правомерно только при замещении первого атома хлора. [30]
Страницы: 1 2 3