Новый асимметрический атом
Cтраница 3
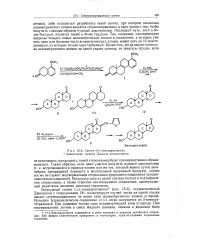 |
Синтез ( у-эпиандростерона. [31] |
Последний путь, хотя и более быстрый, является также и более трудным. Так, например, одновременное введение четырех новых асимметрических атомов в соединение, в котором уже есть один или большее число асимметрических атомов, может дать до 16 диасте-реомеров, из которых только один требуемый. [32]
Более сложная картина возникает в том случае, когда карбонильная группа связана с асимметрическим центром. Присоединение ведет к образованию диастереомера, образующегося при появлении нового асимметрического атома углерода. Для предсказания его конфигурации используется следующее правило. Для исходного кетона строится проекция Ньюмена вдоль связи, соединяющей карбонильный углерод с асимметрическим. [33]
При взаимодействии любого из глицериновых альдегидов с синильной кислотой асимметрический атом исходного альдегида не вовлекается в реакцию и переходит с сохранением пространственной конфигурации соединенных с ним групп в образовавшийся оксинитрил, а из него при дальнейших превращениях - в альдотетрозу. Однако при превращении карбонильной группы глицеринового альдегида в оксинитриль-ную возникает новый асимметрический атом ( стр. [34]
При взаимодействии любого из глицериновых альдегидов с синильной кислотой асимметрический атом исходного альдегида не вовлекается в реакцию и переходит с сохранением пространственной конфигурации соединенных с ним групп в образовавшийся оксивитрил, а из него при дальнейших превращениях - в альдотетрозу. Однако при превращении карбонильной группы глицеринового альдегида в оксивитрильную возникает новый асимметрический атом ( стр. [35]
В литературе нет единого мнения относительно определения этих терминов. В настоящей книге они будут равноправно употребляться для обозначения образования кап нового асимметрического атома, так и целой диссимметричной молекулы в условиях, при которых два стереоизомера образуются в неравных количествах. [36]
Следует заметить, что хотя все три углеводорода С10Н18 правовращающие, однако углы вращения у них различны. Причина такого различия вполне понятна, если учесть, что при гидрогенизации левовращающего а-туйена появляется новый, асимметрический атом углерода. [37]
Как уже было указано выше ( см. стр. Наоборот, если новый асимметрический атом углерода появляется в оптически деятельном веществе, то отношения двух антиподных конфигураций нового асимметрического атома ( abc и асЪ на рис. 38) к ранее имевшейся системе асимметрического атома ( хуг) будут неодинаковы. [38]
Как уже было указано выше ( см. стр. Наоборот, если новый асимметрический атом углерода появляется в оптически деятельном веществе, то отношения двух антиподных конфигураций нового асимметрического атома ( abc и acb на рис. 38) к ранее имевшейся системе асимметрического атома ( xyz) будут неодинаковы. [39]
Если при химических синтезах из веществ с симметричными молекулами создаются вещества с асимметрическим атомом углерода, то они получаются в виде недеятельных соединений. Однако, пользуясь оптически деятельными веществами, можно в некоторых случаях из веществ, не содержащих асимметрического атома углерода, получить оптически деятельные вещества. Для этого исходное вещество связывают с оптически деятельным веществом и удаляют последнее после того, как путем химической реакции получен новый асимметрический атом. Так можно синтезировать оптически деятельную молочную кислоту СН3 - СН ( ОН) - СООН из пировиноградной кислоты СН3 - СО-СООН, в молекуле которой нет асимметрического атома. [40]
Synthese im asymmetrischen Sinne), по-видимому, впервые применив этот термин. По его предположению, в подобного рода синтезе уже имеющиеся асимметрические атомы углерода обусловливают возникновение только одного из двух, казалось бы, возможных, асимметрических атомов углерода. Представлял поэтому принципиальный интерес такой асимметрический синтез, когда новый асимметрический атом углерода мог быть отделен в составе производной молекулы от остальных асимметрических атомов. С другой стороны, не менее интересно было выяснить и механизм образования такого нового атома углерода. [41]
Бензилиденовые производные Сахаров, так же как и рассмотренные выше изопропилиденовые производные, нашли широкое применение в синтетической химии углеводов. Стереохимические требования к реакции бензальдегида с сахарами несколько иные, чем для ацетона. Отличие состоит в том, что бензальдегид предпочтительнее реагирует с ( З - гликоль-ными группировками и образует ж-диоксановый цикл. Кроме того, бензил-иденовый остаток может быть удален не только кислотным гидролизом, но и в нейтральной среде гидрогенолизом над катализаторами платиновой группы. После присоединения бензилиденового остатка в молекуле моносахарида возникает новый асимметрический атом углерода и в ряде случаев получающиеся диастереомеры могут быть разделены. Однако в тех случаях, когда бензальдегид реагирует с образованием м-диоксано-вого цикла, обычно образуется только один диастереомер, в котором фенильный остаток занимает экваториальное положение. [42]
Если синильной кислотой действовать на глицериновый альдегид, уже содержащий две гидроксигруппы, получается тригидроксинитрил. Рассмотрим эту реакцию, взяв в качестве исходного D-глицериновый альдегид. Он содержит один асимметрический атом. В результате же присоединения HCN углерод его карбонильной группы также становится асимметрическим и в образующемся тригидроксинит-риле оказываются два асимметрических углерода. Получаются две диастереомер-ные формы тригидроксинитрила ( I и II), отличающиеся положением групп ОН и атомов Н при новом асимметрическом атоме. Это объясняется тем, что в процессе присоединения HCN и разрыве двойной связи между С и О углерод карбонильной группы, становясь асимметрическим, с одинаковой вероятностью получается в двух возможных пространственных конфигурациях. [43]
Рассмотрим эту реакцию, взяв в качестве исходного - D-глицериновый альдегид. Он содержит один асимметрический атом. В результате же присоединения HCN углерод его карбонильной группы также становится асимметрическим, и в образующемся триоксинитриле будет два асимметрических углерода. Получаются две диасте-реоизомерные формы триоксинитрила ( I и II), отличающиеся положением групп ОН и атома Н при новом асимметрическом атоме. Это объясняется тем, что в процессе присоединения HCN и разрыва двойной связи между С и О углерод карбонильной группы, становясь асимметрическим, с одинаковой вероятностью получается в двух возможных пространственных конфигурациях. [44]
При рассмотрении взаимодействия между гексозами и фенил-гидразином было установлено, что глюкоза и фруктоза образуют один и тот же озазон и что из этого озазона путем гидролиза и осторожного восстановления получающегося при этом озона можно получить фруктозу. Это было, таким образом, случаем превращения глюкозы в фруктозу, глюкоза - - глюкозазон - глюк-озон - фруктоза. Для этого фруктозу нужно восстановить в соответствующий гексит. В молекуле фруктозы три асимметрических атома ( карбонильная форма), в полученном из нее гексите четыре, так как при восстановлении карбонильной группы в спиртовую создается новый асимметрический атом. [45]
Страницы: 1 2 3 4