Емкостная кривая
Cтраница 3
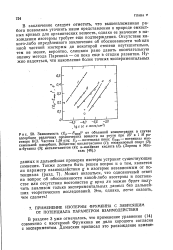
Влияние природа катиона отражается на форме и положении ЭКК и емкостных кривых. Из положения ЭКК и значений QmaK видно, что лля IH. Cfmaj ( наблюдается при 15 - 20 0 и при 45 - 50 С - для СаС1й, Самое низкое значение б по. [31]
Принято считать, что быстрое возрастание емкости на крайних анодных ветвях емкостных кривых - связано с протеканием процесса ионизации ртути. Процесс этот облегчается в присутствии анионов, образующих трудно растворимые соли ртути. [32]
Принято считать, что быстрое возрастание емкости на крайних анодных ветвях емкостных кривых связано с протеканием процесса ионизации ртути. Процесс этот облегчается в присутствии анионов, образующих трудно растворимые соли ртути. [33]
Это и определяет очень высокие емкости и большую температурную зависимость в анодной области емкостных кривых для концентрированного С ( г Для более гидратированных катионов / ffi и К эти аффекты выражены значительно слабее ( рис. б), что подтверждает нашу точку зрения. [34]
 |
Иллюстраций 8. Библ. 14 назв. [35] |
Переходу от первой адсорбционной предволны ко второй на подпрограмме соответствует пик дополнительной емкости на емкостной кривой в связи с переориентацией I в адсорбционном слое согласно предположению Зумана и Ход-ковского. [36]
В заключение следует отметить, что вышеизложенная работа позволила уточнить наши представления о природе емкостных кривых для органических веществ, однако ее значение в на хождении изотермы требует еще подтверждения. Отсутствие какого-либо определенного заключения об обоснованности той или иной частной изотермы до некоторой степени неутешительно, тем не менее, вероятно, слишком рано давать окончательную оценку метода Парсонса - он пока еще в стадии развития. [38]
Переходу от первой адсорбционной предволны ко второй на поляризационной кривой соответствует пик ( переориентация дитро-пила в адсорбционном слое) на емкостной кривой. При потенциалах предельного тока третьей предволны емкость достигает самых низких значений в результате образования полимолекулярного слоя дитропила в соответствии с предложением Зумана и Ходковского. При потенциале перехода к предельному диффузионному току емкость повышается до уровня, соответствующего мономолекулярному слою. Предполагается, что скорость восстановления катиона тропилия увеличивается при этом значении потенциала в результате либо разрушения полимолекулярного слоя дитропила, либо ускорения проникновения катионов тропилия через пленку дитропила. В присутствии поверхностно-активных анионов ( J -), которые ускоряют восстановление катиона тропилия в интервале потенциалов второй и третьей адсорбционных предволн, емкость снижается в результате адсорбции дитропила до величины, соответствующей мономолекулярному слою. Первая адсорбционная предволна в этом опыте обнаруживает свойства предволны Брдички. [39]
Поскольку упомянутые выше работы Грэма отражают развитие исследований емкости в этот период, можно заметить, что техника и методика получения емкостных кривых на ртути быстро усовершенствовались и этот метод был затем использован для исследования структуры двойного слоя. [40]
В заключение следует отметить, что метод расчета Дамаски-на определенно удачен при описании адсорбции на основании изотермы Фрумкина, однако согласие с экспериментальными емкостными кривыми достигается благодаря введению завися1 - щего от потенциала параметра взаимодействия. Остается рассмотреть, будут ли некоторые другие изотермы в табл. 5 так же хорошо соответствовать экспериментальным результатам, как изотерма Фрумкина, при условии что вводится зависящий от потенциала параметр. [42]
Опыт показывает, что при повышении температуры от 20 до 60 С, которое сопровождается увеличением высоты суммы адсорбционных пред-волн тропилия [2], емкостная кривая заметным образом не изменяется. Следовательно, рост адсорбционных волн в этом случае связан с ускорением либо удаления дитропила с поверхности электрода, либо проникновения катиона тропилия через пленку дитропила, структура которой сохраняется такой же. [43]
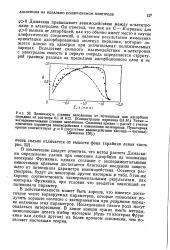
Оставляя в стороне детали емкостных кривых, обратим внимание на главное: как при низких ( рис. 4), так и при высоких концентрациях иодид-иона ( рис. 5) их адсорбция не составляет непреодолимого препятствия для адсорбции дитропила: в широком интервале потенциалов на емкостных кривых наблюдается депрессия, обусловленная, как и прежде, адсорбцией дитропила. [44]
Макдональд и Барлоу разработали модель с учетом этих двух эффектов и детально рассчитали ее. Теоретические емкостные кривые очень хорошо соответствуют экспериментальным кривым для д0, однако этого согласия не наблюдается, если q становится более положительным. [45]
Страницы: 1 2 3 4 5