Емкостная кривая
Cтраница 5
Даже при небольшом удалении от потенциала нулевого заряда в катодном направлении свойства адсорбционного слоя дитропила существенно изменяются: емкость заметно повышается, причем в переходной области потенциалов ( около - 0 7 б) на кривой всегда образуется небольшой пик. Как раз на потенциал переходной области приходится резкий переход к плато предельного диффузионного тока на полярограмме тропилия: скорость процесса возрастает. Мы зарегистрировали емкостные кривые раствора перхлората тропилия ( - 10 - 3 М) при измерении в различные моменты жизни капли ( от 0 7 до 4 сек) и нашли, что изменение величины задержки в этих пределах не оказывает существенного влияния на эффекты от адсорбции и катионов тропилия и дитропила. [61]
 |
Кривые дифференциальной емкости ртути в этгшоловых растворах серы на фоне 1М. [62] |
Кривая О отвечает раствору, не содержащему серы. Добавление серы вызывает несколько эффектов на емкостной кривой. Рассмотрим отдельные участки емкостной кривой раствора серы. [63]
В области потенциалов адсорбции дитропила, устанавливаемой по емкостным и электрокапиллярным измерениям, как уже отмечалось, на поляризационных кривых растворов соли тропилия наблюдаются три адсорбционные предволны и диффузионная волна с резким выходом на плато предельного тока. Эти особенности поляризационной кривой также находят соответствующее отражение на емкостных кривых. Зумана и Ходковского [5], на емкостной кривой возникает небольшой пик. Если бы в действительности имела место не переориентация молекул дитропила, а просто утолщение слоя с сохранением ориентации ( наслоение), то, вероятно, на емкостной кривой пик не появился, а наблюдалось бы дальнейшее снижение емкости. Следовательно, емкостные измерения находятся в соответствии с этим предположением Зумана и Ходковского. [64]
Повышение емкости в связи с адсорбцией катиона тропилия сравнительно невелико. По всей видимости, оно связано с началом пика переориентации катионов тропилия, как это трактуется и для ароматических углеводородов. По мере увеличения положительного заряда поверхности ртути емкостные кривые катиона тропилия все меньше отличаются от кривой фона, что также характерно для поведения ароматических соединений. [65]
Макдональдом и Барлоу специфической адсорбцией фтор-иона; возможно, что в пользу этого объяснения говорят расхождения, полученные Грэмом - между экспериментальными значениями емкости и значениями, рассчитанными на основании теории Гун - Чапмана при предположении об отсутствии специфической адсорбции ( гл. Макдональд и Барлоу недавно заметили [65], что источником расхождения является неучет дискретности молекул растворителя и их поляризация в поле. Они тщательно разработали идею своей первоначальной работы в двух последних статьях и улучшили согласие экспериментальных и теоретически рассчитанных емкостных кривых. [66]
 |
Сопоставление полярограмм ( а и. [67] |
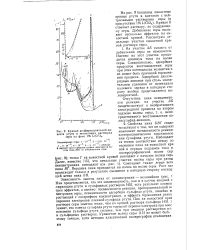
Если адсорбционная природа действияповерхностно-активных анионов несомненна, то еще неясно, изменяют ли анионы свойства адсорбционной пленки ди-тропила. На рис. 4 в одной и той же шкале потенциалов сопоставлены три серии кривых: полярограммы раствора бромистого тропилия с добавками NaJ, емкостные кривые тех же растворов и емкостные кривые таких же растворов NaJ, но в отсутствие соли тропилия. [68]
Так, были получены [37] электрокапиллярные и емкостные данные для 0 1 N и насыщенных растворов LiNO3 в метаноле и этаноле. При переходе от водных растворов LiNO3 [17, 25] к спиртовым [37] было четко отмечено влияние степени сольватации аниона NO - на изменение величины емкости в минимуме емкостных кривых с концентрацией ( ср. [69]
Если адсорбционная природа действияповерхностно-активных анионов несомненна, то еще неясно, изменяют ли анионы свойства адсорбционной пленки ди-тропила. На рис. 4 в одной и той же шкале потенциалов сопоставлены три серии кривых: полярограммы раствора бромистого тропилия с добавками NaJ, емкостные кривые тех же растворов и емкостные кривые таких же растворов NaJ, но в отсутствие соли тропилия. [70]
Страницы: 1 2 3 4 5