Пиррольный атом - азот
Cтраница 2
В азаиндолах энергия перехода изменена и наиболее важное возмущение вызывается пиррольньш атомом азота. Поскольку пиррольный атом азота дает в общую я-систему молекулы два электрона, он приобретает большую эффективную электроотрицательность и, следовательно, обладает большим инкрементом куло-новского интеграла, возможно сравнимым с инкрементом положительно заряженного азота в ионе пиридиния. Любые другие пиридиновые атомы азота в азаиндолах обладают меньшими инкрементами кулоновского интеграла, равными инкрементам нейтральных атомов азота в шестичленных ароматических циклах. [16]
Различное спектральное поведение производных двух типов азаинденов может возникать вследствие менее полной делокализа-ции я-электронов в индолах. Локализация двух я-электронов у пиррольного атома азота индола приводит к образованию в остальной части молекулы я-электронной системы стирола. Аналогичная локализация я-электронов в пирроле или индолицине приводит к образованию неароматических систем - бутадиена или октатетраена. В этих случаях снижение энергии делокализации должно быть большим. Поэтому можно полагать, что делокализация я-электронов является более полной в ряду ин-долицина по сравнению с рядом индола, что соответствует и большей применимости модели делокализованного аниона индена для объяснения спектров ряда индолицина. [17]
В схеме не указаны имеющиеся в молекуле боковые цепи. В центре находится связанный с пиррольными атомами азота металл: магний в хлорофилле, железо в гемоглобине. Вся структура соединена еще с белковой частью, без которой ни хлорофилл, ни гемоглобин неспособны осуществлять свои биохимические функции. [18]
В схеме не указаны имеющиеся в молекуле боковые цепи. В центре находится связанный с пиррольными атомами азота металл: магний в хлорофилле, железо в гемоглобине. Вся структура соединена еще с белковой частью, без которой ни хлорофилл, ни гемоглобин не способны осуществлять свои биохимические функции. [19]
Коэффициент D определяет ось наибольшего ковалентного связывания или градиента электрического поля, и, следовательно, определяет ось максимального взаимодействия металл - лиганд. Поскольку наибольший вклад в поле лигандов определяется донор-ными пиррольными атомами азота порфирина, ось D, указывающая направление наибольшего взаимодействия металл - лиганд, должна соответствовать направлению, определяемому парой пиррольных атомов азота, расположенных по диагонали относительно координирующего катиона металла. [20]
Следовательно, длинная цепочка фитола не оказывает существенного влияния на эффект фотоиндуцированного парамагнетизма. Феофитин представляет собой безмагниевый хлорофилл с присоединенными вместо магния к пиррольным атомам азота двумя атомами водорода. [21]
В индолах наиболее важное возмущение и связанное с этим поглощение вызывается пиррольным атомом азота, который дает в л-систему молекулы два электрона и в связи с этим приобретающий большой эффективный отрицательный заряд. В спектрах некоторых азотсодержащих производных индола две полосы длинноволнового поглощения маскируются плавной кривой поглощения, в то время как интенсивная полоса имеет гипсохромный сдвиг. [22]
Наклонное расположение координированного азид-иона не допускает эквивалентного взаимодействия орбиталей азота азида с & xz - и с г-орибиталями. Структурные данные [93], подтверждающие, что при связывании азид-аниона происходят малые сдвиги пиррольных атомов азота, обсуждались выше ( разд. [23]
В фуране и тиофене ароматический секстет также включает неподеленную пару электронов негибридизованной р - АО кислорода и серы соответственно. В имидазоле два атома азота вносят разный вклад в образование делокализован-ного электронного облака: пиррольный атом азота поставляет пару п-электронов, а пиридиновый - один р-элект-рон. [24]
Хотя пяти - и шестичленные гетероциклы наиболее распространены, большое значение в гетероароматическом ряду имеют и м акроциклические системы. К ним, в частности, относится порфин ( 30), молекула которого содержит 18 периферических я-электронов ( счет ведется по контуру, охватывающему пиридиновые и исключающему пиррольные атомы азота); общее число я-электронов в порфине равно 26, что также соответствует правилу Хюккеля. [25]
Коэффициент D определяет ось наибольшего ковалентного связывания или градиента электрического поля, и, следовательно, определяет ось максимального взаимодействия металл - лиганд. Поскольку наибольший вклад в поле лигандов определяется донор-ными пиррольными атомами азота порфирина, ось D, указывающая направление наибольшего взаимодействия металл - лиганд, должна соответствовать направлению, определяемому парой пиррольных атомов азота, расположенных по диагонали относительно координирующего катиона металла. [26]
Наличие такого равновесия спиновых состояний свидетельствует о том, что увеличение кооперативного взаимодействия субъединиц гемоглобина в окислительно-восстановительной реакции в щелочных условиях обусловлено восстановлением низкоспинового гидроксометгемоглобина в дезоксигемоглобин. Из зависимости изменения ориентации порфирина от спинового состояния, показанной на рис. 11, следует, что при переходе от высоко - к низкоспиновому состоянию ферригемопротеина происходит поворот порфиринового кольца приблизительно на 2, сопровождающийся размещением атома железа в плоскости пиррольных атомов азота. Это приведет к поступательному движению порфиринового кольца относительно атома железа на - 30 пм. Незначительное изменение ориентации порфиринового кольца, происходящее в результате его поступательного движения и поворота, подчеркивает важную роль малых конформационных изменений третичной структуры белка, сопровождающих изменение стереохимии железопорфирина. [27]
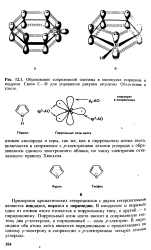 |
Образование сопряженной системы в молекулах пиридина и пиррола. Связи С - Н для упрощения рисунка опушены Обьясненне в тексте. [28] |
Примерами ароматических гетероциклов с двумя гетероатомами являются имидазол, пиразол и пиримидин. В имидазоле и пиразоле один из атомов азота относится к пиррольному типу, а другой к пиридиновому. Пиррольный атом азота вносит в сопряженную систему два / электрона, а пиридиновый - один / - электрон. В пиримидине оба атома азота являются пиридиновыми и предоставляют по одному / 7-электрону в сопряжение с / - электронами четырех атомов углерода. [29]
Гидрирование пиррола ( хлорофиллы) или его окисление ( продукт фотоокисления прото-порфирина) может в результате нарушения сопряжения двойных связей тетрапиррола приводить к образованию соединений зеленого цвета. Спектры таких соединений характеризуются интенсивной полосой поглощения в красной области; другие Хшах ( и е) в видимой области сходны у родственных порфиринов. Гидрирование порфиринового ядра по двум пиррольным атомам азота и по всем атомам углерода метановых мостиков дает порфириногены, промежуточные соединения при биосинтезе порфиринов; известны также родственные не полностью гидрированные порфирины. [30]
Страницы: 1 2 3