Электроотрицательный атом
Cтраница 1
Хотя сильно электроотрицательные атомы галогенов, связанные с углеродом, обычно не выступают в роли нуклеофилов, поскольку при этом они должны были бы проявлять двухвалентность и принять положительный заряд, тем не менее среди первых же примеров участия соседних групп оказались примеры участия брома. [1]
Присоединение электроотрицательных атомов к атому азота увеличивает s - характер свободной электронной пары. Это в свою очередь приводит к дестабилизации переходного состояния по сравнению с основным состоянием и к возрастанию энергетического барьера. Предположили, что причиной подобного изменения энергетических характеристик при замещении гетероатомами являются и другие факторы, включая взаимное отталкивание свободных электронных пар. Однако для нас в данном случае существенно то, что барьер активации действительно возрастает, как это следует из ряда примеров, приведенных в табл. 6 1.1, при замещении алкильной группы атомом хлора. Действительно, значительная дестабилизация переходного состояния в сравнении с основным состоянием происходит при одновременном воздействии двух факторов - напряжения цикла и гетерозамещения. При этом возникает возможность разделять инвертомеры азота [ например, в случае ( 44) методом газожидкостной хроматографии ], хотя в данном случае они являются диастереомерами, а не энан-тиомерами. При асимметрическом хлорировании азиридина ( 47) с помощью оптически активных хлорирующих агентов при низких температурах была получена смесь двух N-хлорзамещенных энантиомеров в неравных количествах ( уравнение 112), обладающая оптической активностью. Присоединение нитрена к стиролу в условиях кинетического контроля протекает етереоизбирательно ( уравнение 113) и приводит только к син-инвертомеру ( 48) в результате сильного притяжения между фенильной и N-фталимидной группами в переходном состоянии. Соединение ( 48) сохраняет свою стереохимическую чистоту при температурах ниже 0 С, обращение конфигурации при азоте происходит лишь при повышении температуры. [2]
Удаление электроотрицательных атомов и групп от двойной связи в присутствии тех же катализаторов платиновой группы приводит к повышению выхода продуктов присоединения. [3]
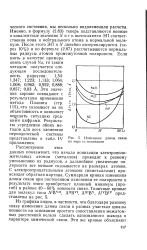 |
Изменение длины связи по мере ее ионизации. [4] |
С электроотрицательными атомами ( неметаллами) происходит обратная картина. Суммарная кривая изменения длины связи при постепенном изменении ее полярности в результате этого приобретает плавный минимум ( прогиб) в районе 40 - 60 % ионности связи. [5]
Растворители, содержащие электроотрицательные атомы ( обычно кислород), сами образуют водородные связи с соответствующими протонами. Образование водородных связей с такими растворителями, как эфиры, спирты, кетоны и др., затрудняет образование как меж -, так и внутримолекулярных водородных связей. [6]
В тетрафторэтене электроотрицательные атомы фтора настолько сильно оттягивают на себя я-электронную плотность, что это соединение способно взаимодействовать даже с таким слабым нуклеофилом, как спирт, и, напротив, неспособно присоединять бромоводород. [7]
В тетрафторэтене электроотрицательные атомы фтора на столько сильно оттягивают на себя л-электронную плотность, что это соединение способно взаимодействовать даже с таким слабым нуклеофилом, как спирт, и, напротив, неспособно присоединять бромоаодород. [8]
 |
К определению контактной разности потенциалов. [9] |
Аналогично адсорбция электроотрицательных атомов на поверхности проводника приводит к существенному повышению работы выхода. Так, адсорбция кислорода на поверхности вольфрама повышает работу выхода примерно на 1 эв. [10]
Для переброса электроотрицательного атома в междуузлия требуется большая работа; по-видимому, именно по этой причине такие случаи фактически не наблюдаются. Второй случай также характеризуется удалением иона из узла решетки, но на этот раз речь идет о положительном ионе, например меди в закиси меди. Для обеспечения электронейтральности металлический атом по соседству с пустым узлом должен нести избыточный положительный заряд. Последний не закреплен и может рассматриваться как движущийся по орбите вокруг пустого узла. При повышенных температурах положительный заряд не локализован около дефекта и может перемещаться по решетке, обусловливая дырочную проводимость. [11]
В присутствии электроотрицательного атома потенциальный ящик в простейшей модели СЭ изображают, как показано на рис. П-5. Атом азота находится в центре ямы. [12]
 |
Участие шапиронов. [13] |
Взаимная ориентация электроотрицательных атомов, облегченная наличием комплементарных сайтов, способствует образованию большого числа водородных связей. [14]
Под влиянием электроотрицательного атома йода электронная плотность в молекуле альдегида начинает смещаться в направлении, указанном стрелкой. Связь между СН3 и Н прочнее, чем связи СН3 - I и Н-I, поэтому в результате образуется молекула метана, а атом йода остается свободным. [15]
Страницы: 1 2 3 4